in vivoイメージング
生物発光イメージングや蛍光イメージングを含むin vivoイメージング技術について、研究における利点、課題、用途とともにご紹介します。
in vivoイメージングとは?
in vivoイメージングとは、生きた個体全体で生物学的プロセスを可視化・研究するためのさまざまな手法の総称です。解剖学的構造、分子・細胞レベルの活動、代謝機能を、個体内でより自然な状態のまま観察することができます。これは、培養細胞内で起こるプロセスを調べるin vitroイメージングとは異なります。
in vivoイメージングの利点:
- 生きた動物から得られた結果は、より生物学的な妥当性が高いこと
- 動物をリアルタイムでモニタリングすることで、腫瘍形成のような動的イベントに関する知見が得られること
in vivoイメージングの課題:
- イメージング装置や動物飼育に高いコストがかかること
- より多くのサンプル数と長い実験期間が必要になること
in vivo生物発光イメージング
生物発光イメージング(BLI)は、生きた個体内の細胞・分子レベルのプロセスをリアルタイムでモニタリングするための非侵襲的な手法です。造影剤や放射線を必要とする他のイメージング手法とは異なり、BLIは生物発光反応によって産生される光のみを利用します。
in vivo 生物発光イメージングの利点
- 非毒性:被験動物に大きなダメージを与えることなく、繰り返しイメージングが可能です。これにより、疾患の進行や遺伝子発現パターンを追跡する縦断的研究が行えます。
- 高感度:ルシフェラーゼ-ルシフェリン反応は効率が高く、バックグラウンドノイズを最小限に抑えながら強い発光シグナルを生成します。この高感度により、ごく低レベルの生物学的活性も検出できます。
in vivo 生物発光イメージングの仕組み
in vivo BLIには、主に以下の3つの構成要素が必要です。
- ルシフェラーゼレポーター遺伝子を発現する動物モデル
- ルシフェラーゼ基質
- イメージングシステム
in vivo BLIの一般的なプロセスは以下の通りです。
- レポーター動物モデルの作製:NanoLuc®やホタルルシフェラーゼなどのルシフェラーゼレポーターを発現する動物モデルを、遺伝子工学的手法によって作製
- 基質の投与: ルシフェラーゼ基質を、通常は注射により動物へ投与
- 発光シグナルの生成:基質が酸素およびATP存在下でルシフェラーゼに接触すると、酵素反応により発光を生じる
- 検出とイメージング:専用のイメージングシステムで発光シグナルを検出し、画像に変換
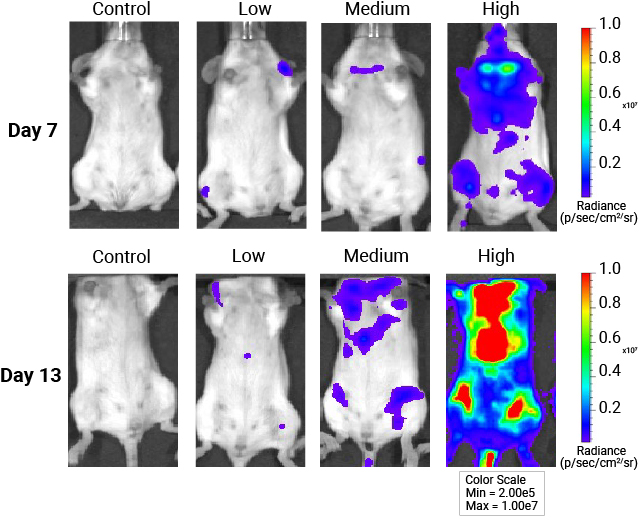
in vivo 生物発光イメージング用レポーターと基質
ルシフェラーゼレポーターから生成される発光シグナルは基質に依存するため、適切な基質の選択が重要です。プロメガでは、以下の各レポーターに最適化した基質を提供しています。
- NanoLuc®ルシフェラーゼの検出:Nano-Glo® Fluorofurimazine In Vivo Substrate (FFz) は、NanoLuc®ルシフェラーゼ、NanoLuc®融合タンパク質、または再構成NanoBiT®ルシフェラーゼのin vivo検出に特化して設計されています。
- ホタルルシフェラーゼの検出:VivoGlo™ Luciferin, In Vivo Grade は、ホタルルシフェラーゼ、ホタルルシフェラーゼ融合タンパク質、または再構成ホタルルシフェラーゼ複合体のin vivo検出に最適化されています。
- NanoLuc®およびホタルルシフェラーゼのデュアル検出: 各基質の特異性により、NanoLuc®とホタルルシフェラーゼを組み合わせたデュアルルシフェラーゼ分子イメージング研究が可能となり、全身動物レポーターモデルの構築においてさらに多くの選択肢が広がります。
Tracking Two Luciferase Reporters in One Animal
Multiplexing bioluminescent reporters in vivo (such as NanoLuc® Luciferase and firefly luciferase) enables simultaneous tracking of two biological processes in the same animal, eliminating inter-animal variability from separate cohorts. This allows researchers to directly correlate specific dynamic events within a single longitudinal study.
See how multiplexing is applied in this publication: Kinase-Modulated Bioluminescent Indicators Enable Noninvasive Imaging of Drug Activity in the Brain
NanoLuc®ルシフェラーゼで生きた動物の脳をイメージング
Nano-Glo® Cephalofurimazine(CFz9)In Vivo Substrateは、生きた動物の脳内でNanoLuc®ルシフェラーゼを検出することを可能にします。CFz9は血液脳関門を通過するよう設計されており、中枢神経系の生理・解剖学的構造の非侵襲的な探索や、脳への治療薬分布の研究を実現します。

CFz9基質の詳細については、こちらのウェビナーをご覧ください。
In Vivo 生物発光イメージングの応用
感染症ダイナミクスの研究
発光細菌やウイルスを用いることで、生きた個体内での感染の広がりと局在をリアルタイムかつ非侵襲的にモニタリングできます。病原体量、体内での拡散、および宿主の免疫応答を経時的に評価することが可能となり、疾患メカニズムや治療介入の有効性に関する知見が得られます。
がんの進行
ルシフェラーゼを発現するよう改変された腫瘍細胞をin vivoで追跡することで、腫瘍量と転移の広がりを縦断的に可視化・定量化できます。この手法は、抗がん療法の有効性評価、腫瘍再発のモニタリング、そして本来の腫瘍微小環境におけるがん細胞生物学の研究に活用できます。
遺伝子治療アウトカムの評価
ルシフェラーゼレポーターを遺伝子治療ベクターに組み込むことで、遺伝子導入効率、発現レベル、および治療遺伝子の持続性を非侵襲的かつ経時的に評価できます。リアルタイムモニタリングにより遺伝子治療戦略の最適化が可能となり、標的を絞った持続的な遺伝子発現が確保されます。
新薬・治療法の開発
in vivo BLIにより、生きた動物における薬効、薬物動態、および体内分布をリアルタイムで評価できます。有望な治療候補の迅速なスクリーニングと同定、薬物メカニズムの研究、および投与レジメンの最適化が可能となります。
in vivo蛍光イメージング
in vivo蛍光イメージング(FLI)は、外部光源による励起によって発光する蛍光プローブまたはリガンドを利用した手法です。
in vivo蛍光イメージングの利点
- マルチプレックス解析:タンパク質や遺伝子ターゲットの同定に利用できる蛍光プローブが幅広く揃っており、多様なマルチプレックスの可能性を実現
- 迅速な解析:蛍光リガンドが産生する光子数が多いため、短い露光時間で画像を取得でき、蛍光マーカーの迅速な解析が可能
in vivo蛍光イメージングの課題
- 自家蛍光:組織由来の自然蛍光が蛍光プローブのシグナルに干渉し、コントラストや精度を低下させる可能性
- 光退色(フォトブリーチング):長時間の光照射により蛍光分子の発光能が低下し、時間の経過とともにイメージング品質が低下。そのため、長期的なキネティクス解析には適さない場合があります。
- 毒性:一部の蛍光色素やプローブは生体組織に毒性を示し、サンプルの生存率や結果の精度に影響を与える場合があります。
in vivoイメージング用HaloTag®リガンド
JFX色素を含むJanelia Fluor® HaloTag®リガンドは、生細胞および内在性環境におけるHaloTag®融合タンパク質の解析用に設計されています。これらの色素は可視光スペクトル全域をカバーし、独自のフルオロジェニック特性を持つことで、高解像度イメージングアプリケーションにおける輝度の向上とバックグラウンドシグナルの低減を実現します。

シナプスタンパク質ターンオーバーの脳全体測定により、学習時の局所的可塑性を明らかに | bioRxiv
引用文献
関連資料
ウェビナー:動的な生物学研究のための生物発光イメージングを習得する
in vivo生物発光イメージングの3つの基本要素である、生物発光レポータータンパク質、レポーター基質、検出装置について学べます。
記事:in vivo生物発光イメージングを使いこなす
in vivo生物発光イメージングは、始めるにあたってハードルが高く感じられることもあります。本記事では、in vivo生物発光イメージングに関して知っておくべきことを網羅的に解説しています。

ポスター:マウスにおけるAAV体内分布の評価
NanoLuc® レポーターを用いることで、生体動物におけるAAV感染組織のウイルスタイターを、ハイスループットかつシンプルな1日ワークフローで測定できる方法をご紹介します。
Interested in more physiologically relevant research tools?
Explore our full portfolio of tools for detecting biologically relevant protein dynamics and cellular activity.