GPCR研究ソリューション
Gタンパク質共役受容体(GPCR)は、最も重要な薬物標的のクラスの1つです。使いやすい生物発光ベースのアッセイを使用して、GPCRシグナル伝達カスケードの各ステップに沿った応答を測定する方法をご用意しています。
研究の課題解決をお手伝いできることを楽しみにしています。何か質問があれば、お気軽にお問い合わせください!

Learn how NanoBRET® technology is used to study the effects of drugs on GPCRs.
GPCR:薬剤開発の要となる存在
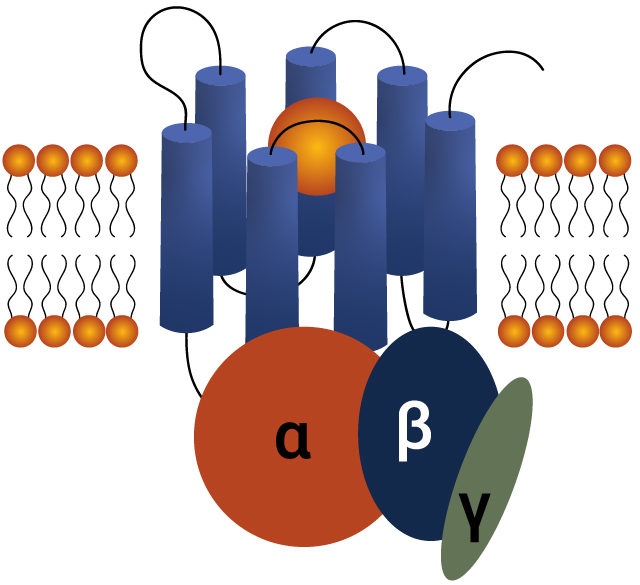
リガンド結合の解析
生細胞内でリガンド結合を測定
NanoBRET® target engagement はリガンド結合を測定するための高感度かつ定量的な手法です。この手法では、GPCRに HiBiT tag (一過性発現またはCRISPR/Cas9によって)を付加、一方でリガンドには蛍光色素を付加します。リガンドがGPCRに結合すると、両者の近接によりエネルギー転移が起こり、蛍光シグナルが生じます。これにより、リガンド結合の精密な定量が可能となります。
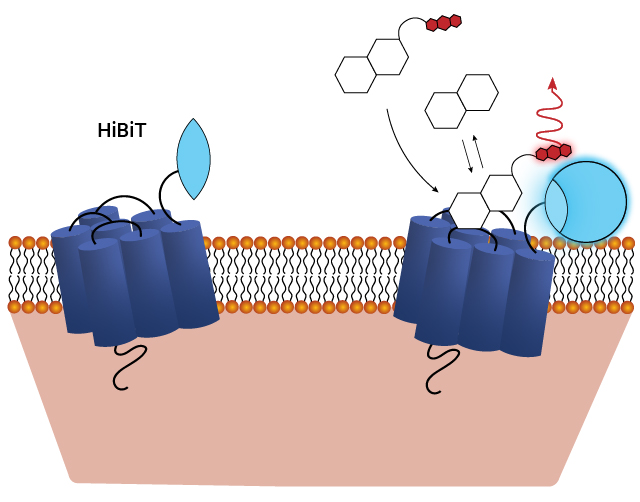
HiBiT/LgBiTレポーターを用いて、BRETを介したリガンドエンゲージメントのモニタリングの模式図 詳細は以下の論文をご参照ください: The luminescent HiBiT peptide enables selective quantitation of G protein–coupled receptor ligand engagement and internalization in living cells.

クロビザンNanoBRET®トレーサーによるαアドレナリン受容体ファミリー5種類のGPCRへの結合飽和 詳細は以下の論文をご参照ください: An integrated approach toward NanoBRET tracers for analysis of GPCR ligand engagement.
GPCRインターナリゼーション
GPCRインターナリゼーションのリアルタイム測定
Nano-Glo® HiBiT Extracellular Detection Systemは、細胞表面に発現しているタンパク質をリアルタイムで定量するための簡便な方法です。この抗体不要のHiBiTタグベースのアプローチにより、受容体の内在化およびその後のリサイクリングを測定でき、抗体法に伴うばらつきを排除することができます。詳細は以下のホワイトペーパーをご参照ください:Quantifying Percent Surface Expression Using Bioluminescent Detection of the HiBiT Protein Tag
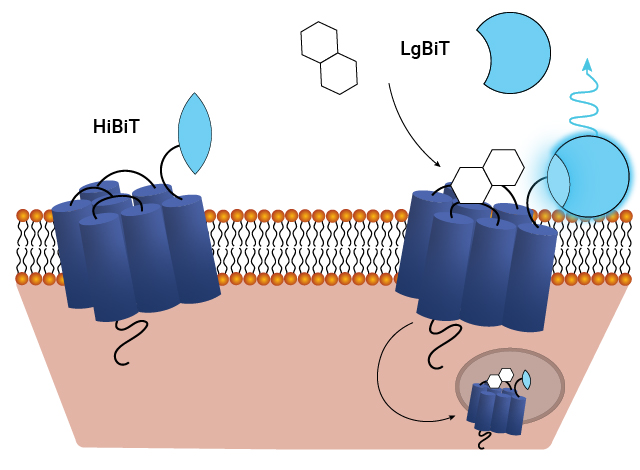
HiBiT/LgBiTレポーターを用いて、リガンド誘導性GPCR内在化をモニタリングするアッセイの模式図 詳細は以下の論文をご参照ください: The luminescent HiBiT peptide enables selective quantitation of G protein–coupled receptor ligand engagement and internalization in living cells.

Nano-Glo® HiBiT細胞外検出システムを用いてモニタリングされたイソプロテレノール依存的内在化 HiBiTタグは、CRISPR遺伝子編集を用いてHEK293細胞のβ2-AR遺伝子に導入されました。
β-アレスチン
β-アレスチンは、受容体の脱感作、内在化の媒介、Gタンパク質非依存的経路の開始を通じて、GPCRシグナル伝達を制御します。GPCRとの相互作用は、シグナル伝達の動態および受容体の輸送を制御する上で重要です。GPCRとβ-アレスチンの相互作用をモニタリングすることは、受容体機能への重要な知見を提供し、特定のシグナル伝達経路を標的とするバイアス型リガンドの創薬に不可欠です。
リアルタイムでGPCR-β-アレスチン相互作用をモニタリング
NanoBiT® Technologyは、複合体形成時に発光シグナルを生成することで、GPCRとβ-アレスチン間のタンパク質間相互作用をリアルタイムかつ定量的に解析することを可能にします。以下のブログにその一例が紹介されています:Bioassay for Cannabinoid Receptor Agonists Designed with NanoBiT® Techology
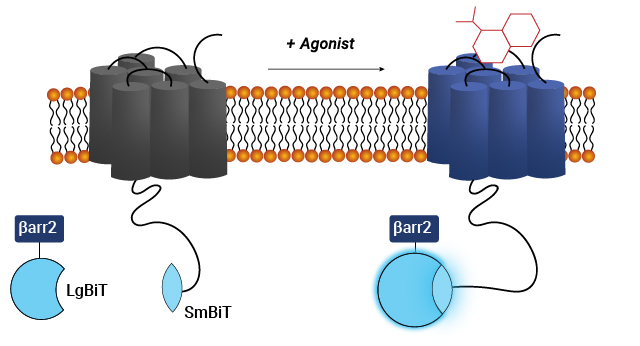
NanoBiT® を利用したβ-アレスチン2 (βarr2)のGPCRへの結合モニタリングの模式図 アゴニストが受容体に結合すると、βarr2がリクルートされ、SmBiTとLgBiTが相互作用して発光シグナルが生じます。


生物発光イメージングによるGPCR-β-アレスチン相互作用の可視化
GloMax® Galaxy Bioluminescence Imager は、GPCRとβ-アレスチン間のタンパク質間相互作用(PPI)を細胞レベルで可視化することができます。この装置は、応答する細胞と応答しない細胞を識別し、細胞集団内での相互作用の速度を明らかにすることで、リアルタイムの生物学的プロセスの視覚的な探索へとデータ収集を進化させます。以下のブログにその一例が紹介されています:Visualize Protein:Protein Interactions with Bioluminescence Imaging(生物発光イメージングによるタンパク質間相互作用の可視化)
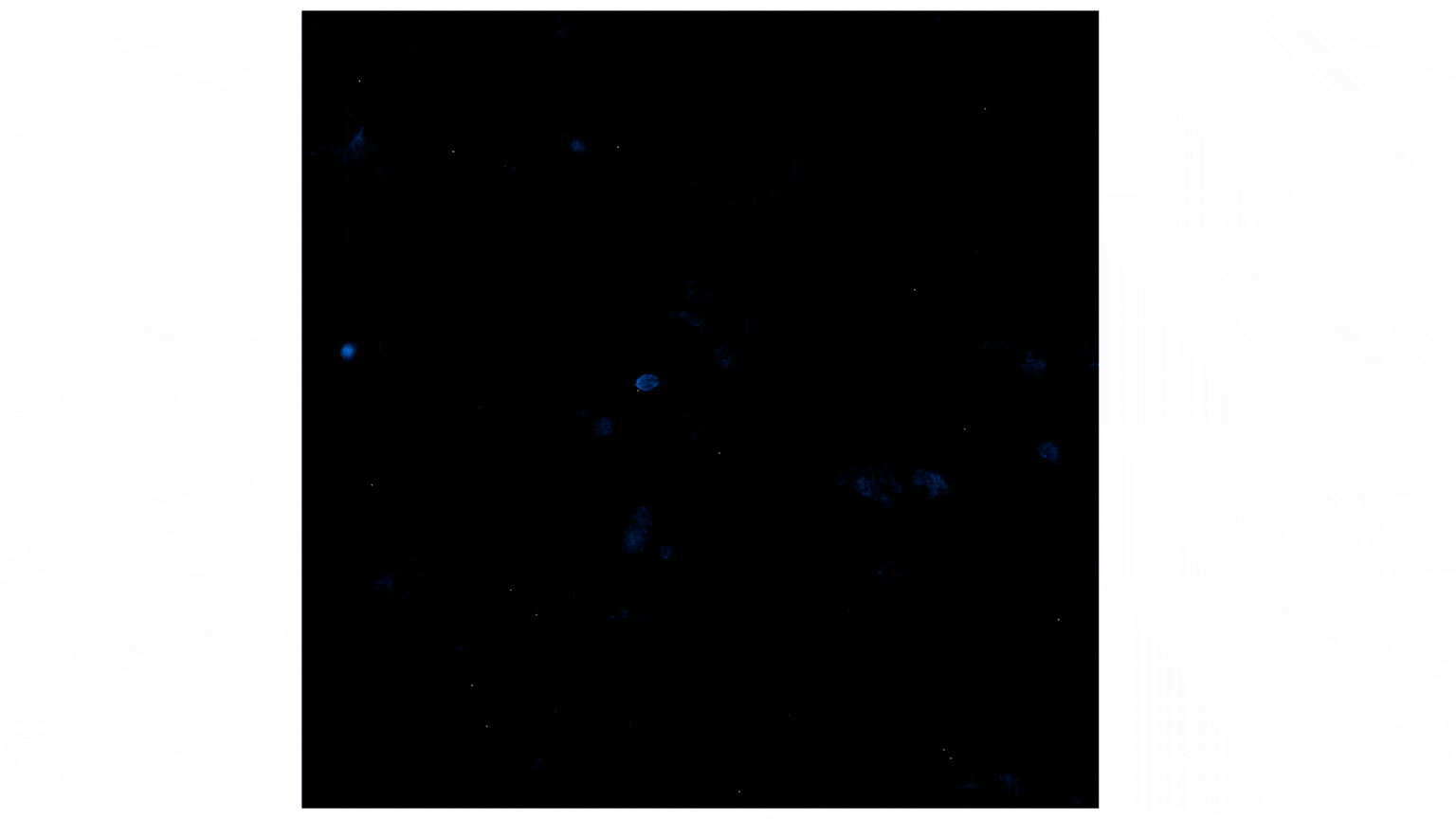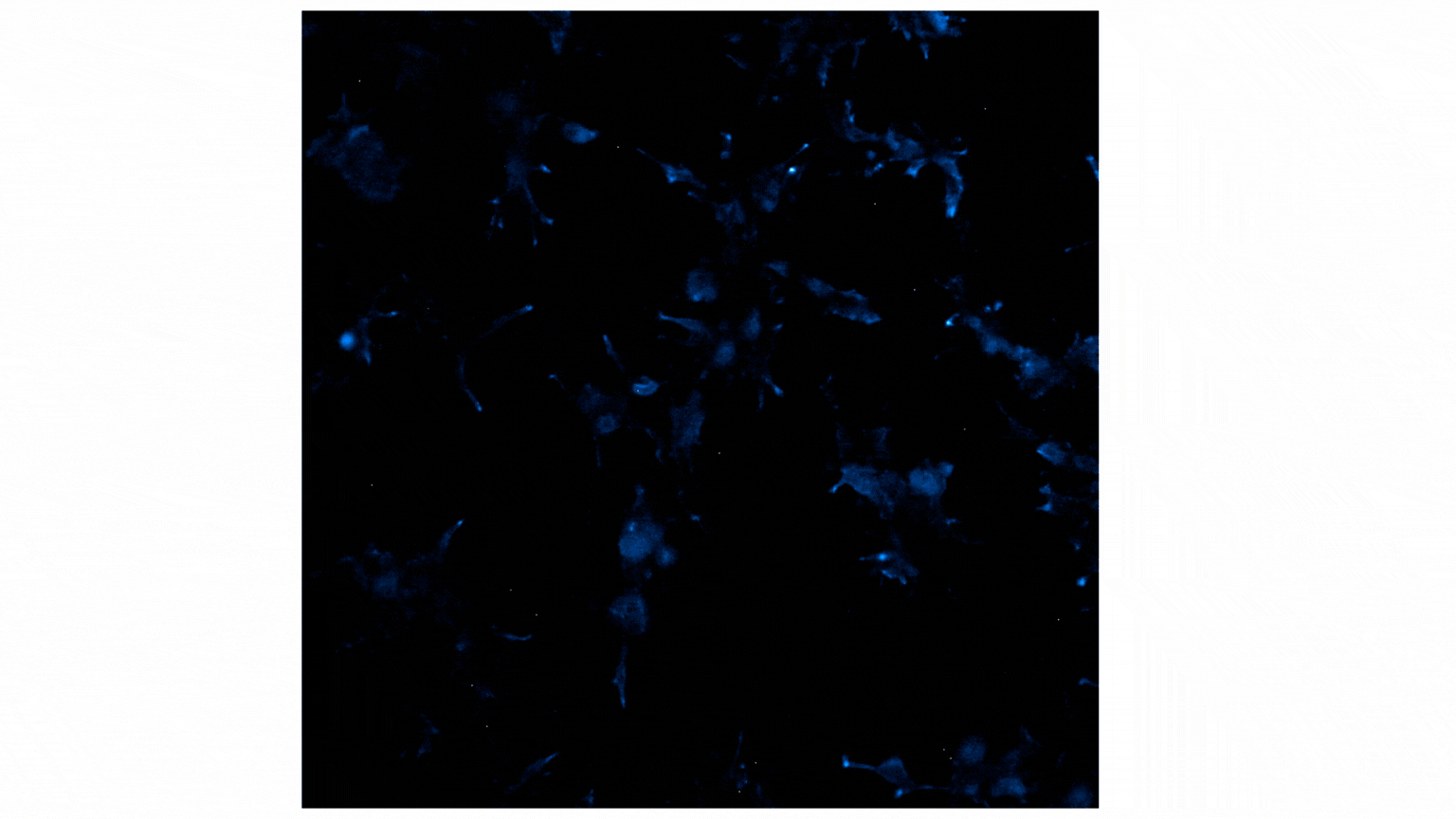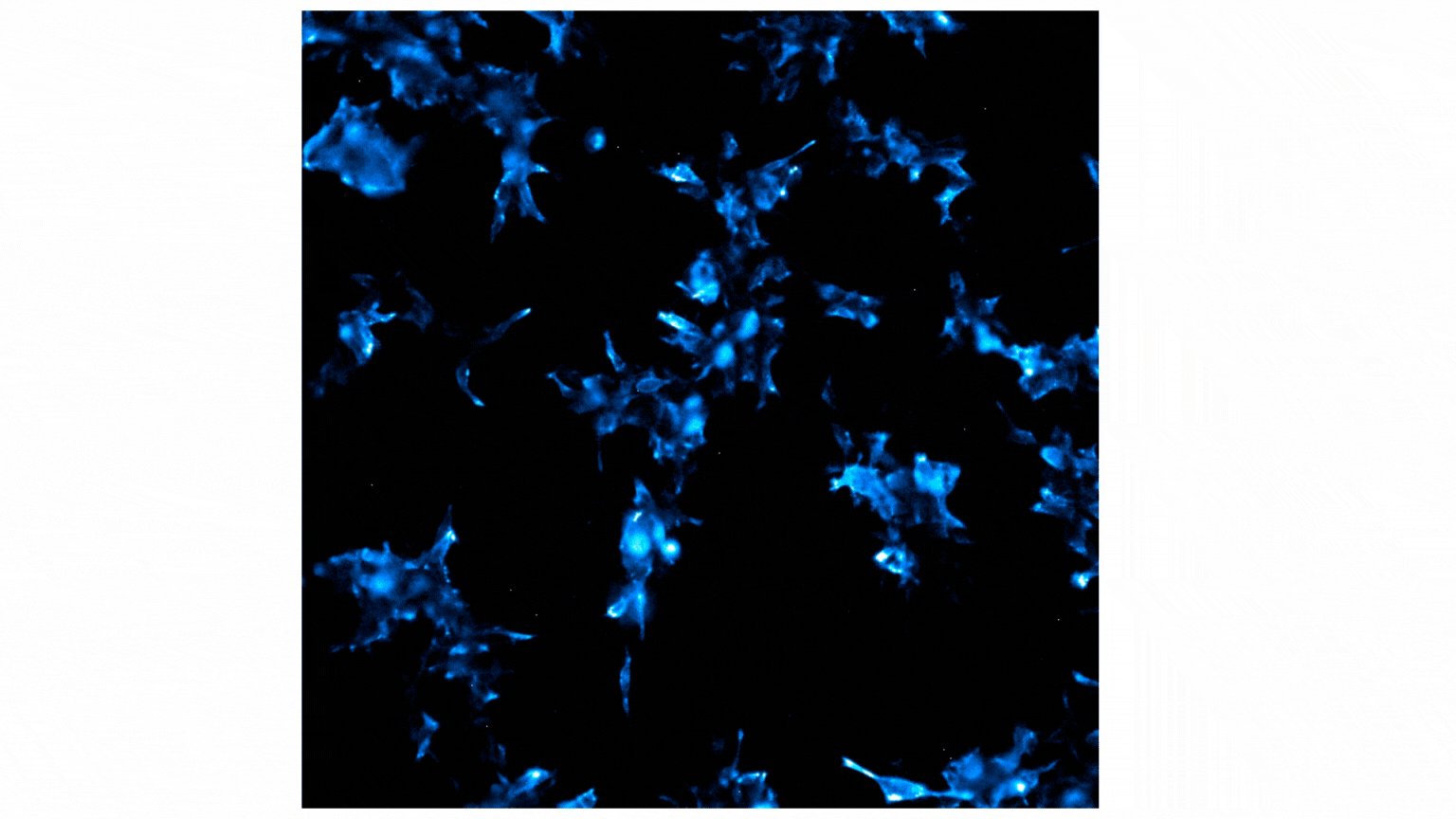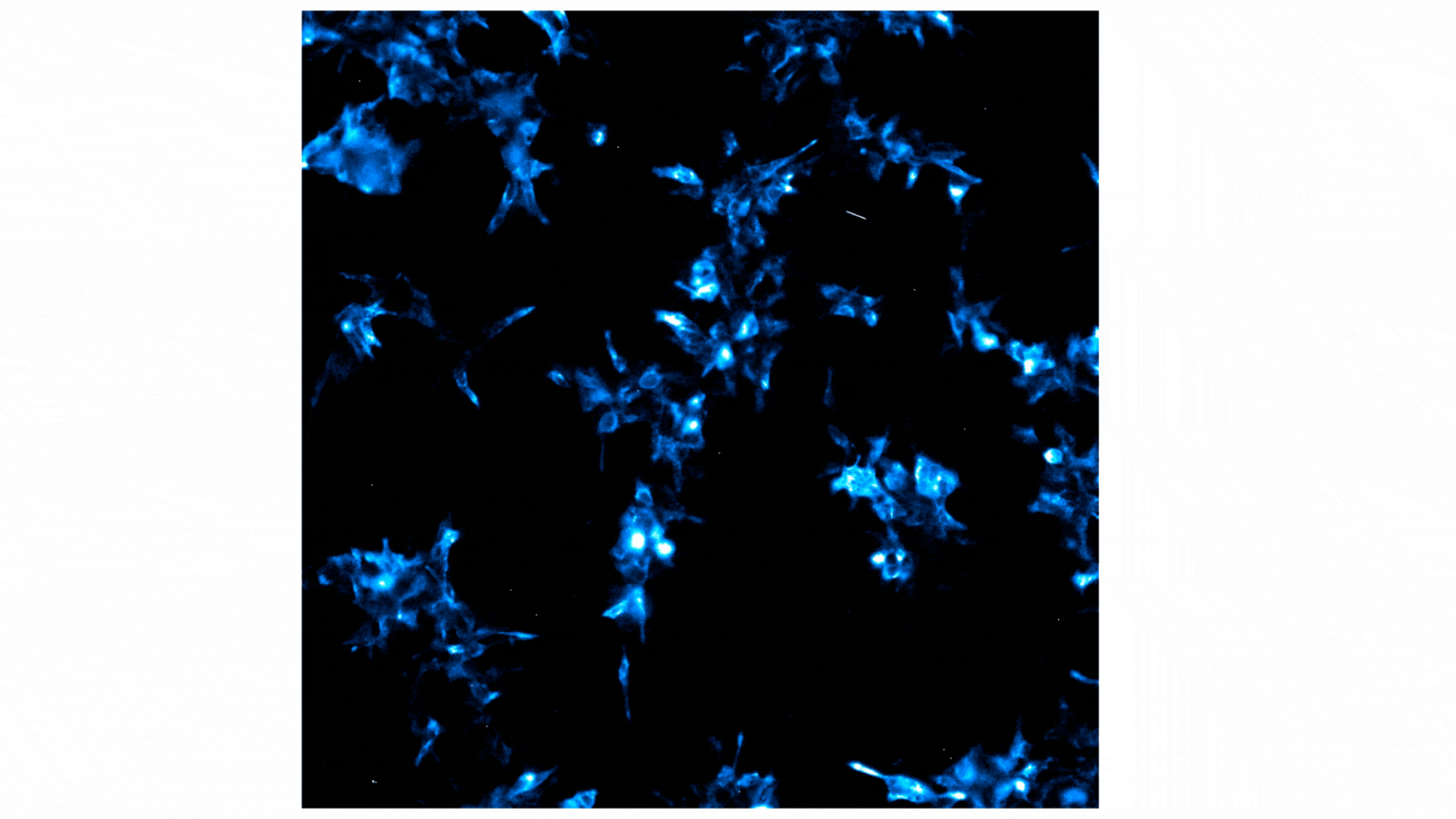
フラクタルカイン処理によりNanoBiT®発光シグナルが増加し、これはCX3CR1とAARB2の相互作用を示しています。局在は主に細胞膜から細胞内の斑点状構造(puncta)へと移行し、受容体の内在化が示唆されます。詳細は以下をご参照ください。ブログ:Visualize Protein:Protein Interactions with Bioluminescence Imaging.
cAMP アッセイ
cAMPやIP3などのセカンダリーメッセンジャーは、GPCR活性化の下流で生成される重要な分子です。リガンドが結合すると、GPCRはGタンパク質を活性化し、アデニル酸シクラーゼやホスホリパーゼCなどの酵素を刺激して、これらのメッセンジャーを産生します。セカンダリーメッセンジャーはシグナルを増幅し、遺伝子発現、代謝、カルシウムシグナリングなど、さまざまな細胞応答を引き起こします。そのため、GPCRを介した経路や薬物作用を理解する上で中心的な役割を担います。
cAMPのハイスループットスクリーニング
Lumit® Technology cAMPを測定するための迅速で洗浄不要の発光ベースアッセイを提供します。この均一系アッセイはワークフローを簡素化し、干渉を最小限に抑え、短時間で正確なハイスループット結果を提供します。
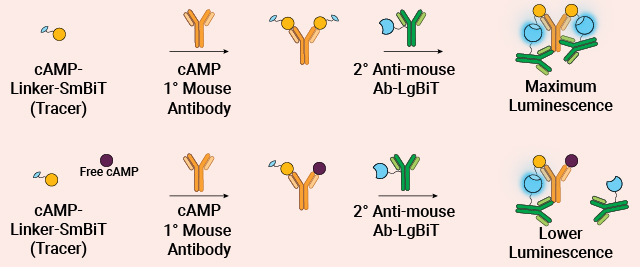

GPCR DRD1の活性を変化させた後のcAMP検出 HEK293細胞にDRD1を安定発現させ、DRD1アゴニストであるドーパミンで処理した結果、cAMPの増加が認められました。詳細は以下の論文をご参照ください:A bioluminescent and homogeneous assay for monitoring GPCR-mediated cAMP modulation and PDE activity(GPCRを介したcAMP変動およびPDE活性のモニタリングのための発光性かつ均一系アッセイ)
細胞ライセート中の細胞内cAMPを測定
cAMP-Glo™ Maxアッセイは、細胞内cAMPを測定するための高感度かつ再現性の高い発光アッセイです。多様なサンプルおよびハイスループットフォーマットに対応しており、シグナルの安定性が高く、干渉も最小限に抑えられるため、信頼性の高い結果が得られます。
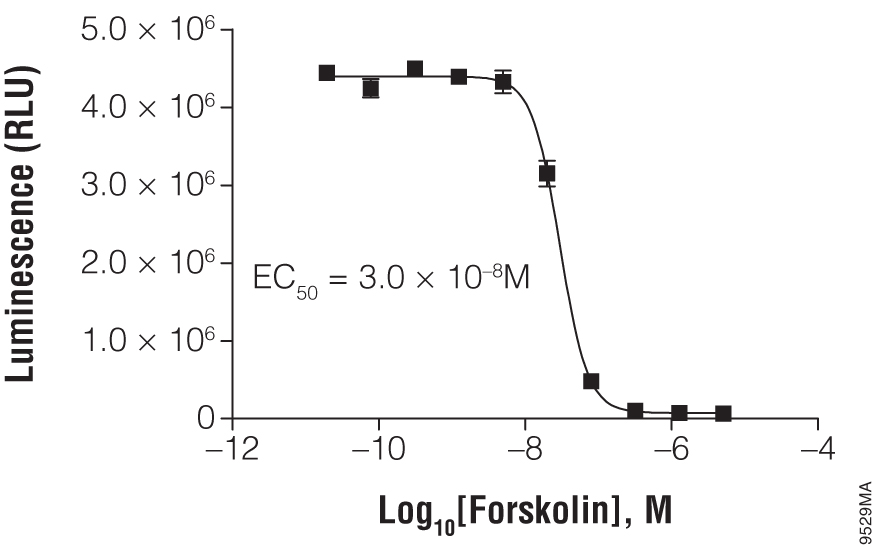
cAMP-Glo™ Maxアッセイを用いたフォルスコリンの滴定
白色・透明底の384ウェルプレートに2,000個のHEK293細胞を播種し、グラフに示す濃度のフォルスコリンで処理しました。
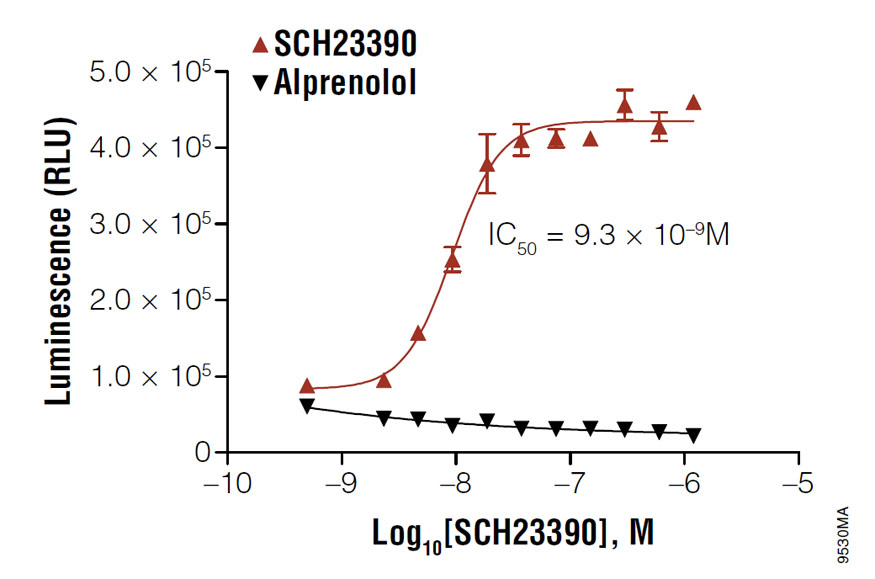
cAMP-Glo™ Max Assay を用いたD1受容体を発現するHEK293細胞におけるSCH23390のIC₅₀値測定 細胞は、100nMのアゴニストSKF38393の存在下で、アンタゴニストSCH23390で処理されました。
生細胞内cAMPのリアルタイム測定
GloSensor™ technology は、ルシフェラーゼを基盤とした柔軟なバイオセンサーのプラットフォームを提供し、生細胞内のシグナル伝達イベントをリアルタイムで、高感度・高直線性・高特異性で検出します。広いダイナミックレンジにより、最大500倍の発光変化を検出することが可能です。非常に高い感度により、化合物(例:フォルスコリン)による人工的な刺激なしに、Gi共役型受容体の活性化やインバースアゴニスト活性を検出することができます。
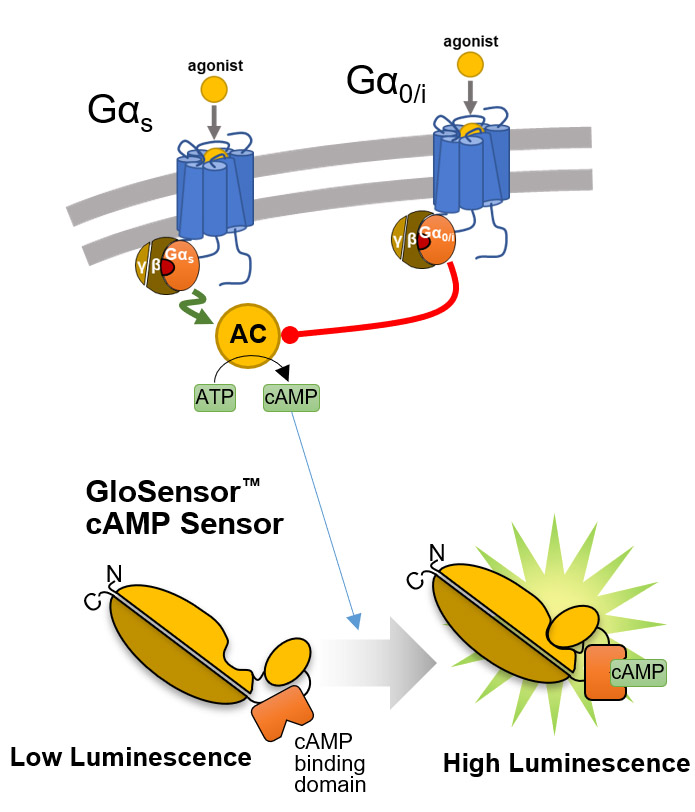
GloSensor™ cAMP Assayの概要 遺伝子導入型バイオセンサーのバリアントは、cAMP結合ドメインと変異型のアメリカホタル(Photinus pyralis)ルシフェラーゼが融合した構造を持ちます。cAMPと結合すると構造変化が生じ、それによって発光量が大きく増加します。
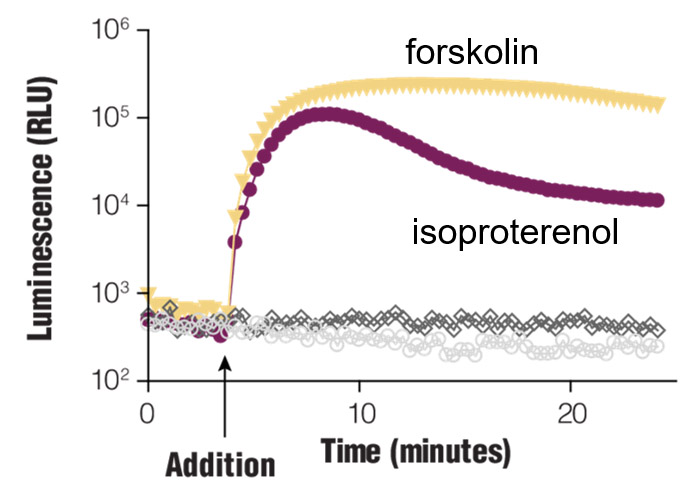
リアルタイムな Gαs モニタリング. pGloSensor™-22F cAMP Plasmid をトランジェントに HEK293細胞にトランスフェクションし、表示の化合物で処理した。
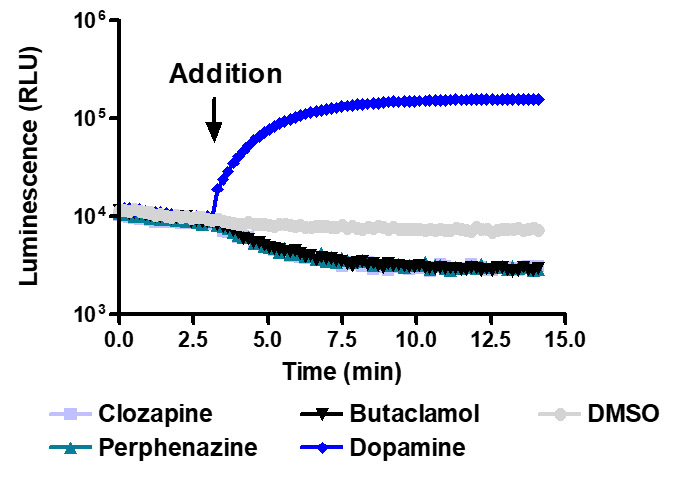
フォルスコリンを用いない受容体逆作動薬検出を可能にする高感度モニタリング. ドーパミン D1 受容体発現 HEK293 細胞に pGloSensor™-22F cAMP Plasmid をトランジェントにトランスフェクションし、28°C で化合物 10µM で処理した。
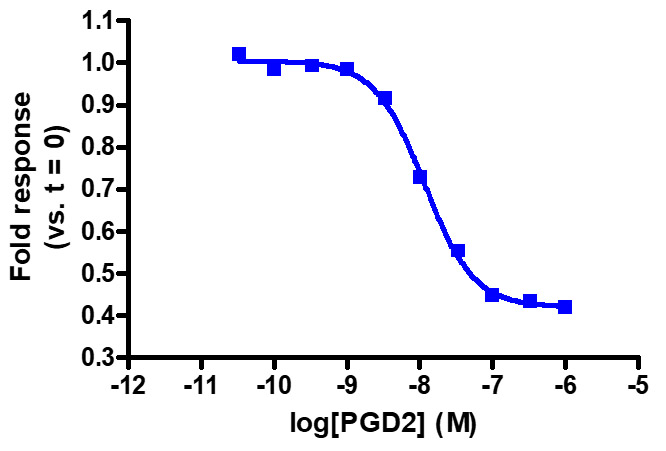
フォルスコリンを用いない Gαi 活性検出を可能にする高感度モニタリング. GPR44 発現 HEK293 細胞に pGloSensor™-22F cAMP Plasmid をトランジェントにトランスフェクションし、プロスタグランジン D2 (PGD2) で処理した。備考:フォルスコリンによる前処理により応答倍率が増加した(データ未掲載)
遺伝子発現
GPCRシグナル伝達は、転写に関与する細胞内経路を活性化することで遺伝子発現を調節します。リガンドが結合すると、GPCRはセカンドメッセンジャーやキナーゼを含むカスケードを引き起こし、転写因子の活性を調節します。このプロセスにより、細胞は環境に適応し、成長、分化、代謝などの重要な機能を制御することが可能になります。
バイオアッセイでGPCRの機能を測定
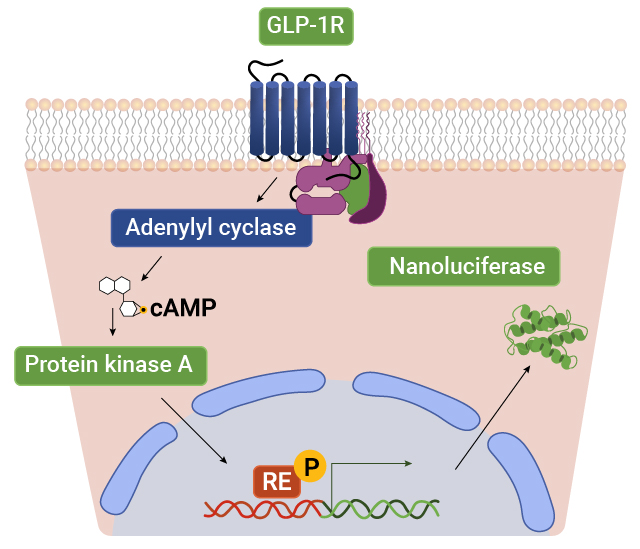
プロメガのバイオアッセイは、細胞表面での受容体活性化が、ルシフェラーゼレポーターに結合された特定の応答エレメントに伝達されるよう設計された細胞を使用しています。リガンドが受容体に結合すると、細胞内のシグナル伝達経路が活性化され、ルシフェラーゼの発現が促進されます。これにより発生する発光シグナルは、受容体活性の高感度かつ定量的な指標となり、GPCR機能およびその下流シグナルの精密な測定を可能にします。
GLP-1、GIP、グルカゴン受容体のアッセイについては Tailored R&D Solutions Team までお問い合わせください。お客様の研究対象となるGPCRに特化したバイオアッセイの作製もサポートいたします!

GLP-1バイオアッセイを用いたGLP-1Rアゴニストの有効性の順位付け 以下のEC50値が測定されました:セマグルチド:52pM、デュラグルチド:38pM、リラグルチド:20pM、エキセナチド:6pM、リキシセナチド:5pM。
レポーターベクターを用いた転写因子の活性化測定
GPCR シグナルのカスケードは遺伝子発現変化の原因となる特定の転写因子の活性化にたどり着きます。ルシフェラーゼレポーターベクターに含まれる応答配列は 、GPCRのシグナルにより伝達された転写因子の活性化をシンプル、高感度で ”添加-混和-測定” だけのシンプルなアッセイを可能にします。

GPCR研究サポートサービス例
GPCR研究をサポートするカスタマイズツールや専門的なガイダンスが必要ですか? Tailored R&D Solutions Team がサポートいたします!提供サービスは以下の通りです:
- アッセイ開発と最適化: GPCRリガンド結合、受容体の細胞内移行、セカンドメッセンジャーの産生など、お客様の研究ニーズに合わせたアッセイを設計します。
- カスタムバイオアッセイ作製: GPCR活性化をルシフェラーゼレポーターで測定可能な細胞株を構築し、受容体活性および下流の遺伝子発現を高精度に測定します。
- 高度な細胞内移行研究: GPCRの細胞内移行や受容体リサイクリングの研究を可能にするツールを提供し、シグナル伝達の調節メカニズムを明らかにします。
- セカンドメッセンジャーおよびキナーゼ経路解析: cAMP、IP3の産生や下流のキナーゼ活性化など、GPCRを介したシグナルの測定を支援します。
- 包括的サポート: GPCRや他の受容体ベースの研究における新たな応用に向け、弊社の科学者と連携して技術の適用を進めることが可能です。
Explore our easy-to-use, bioluminescence-based assays for GPCR research.