NanoBRET® ターゲットエンゲージメント
細胞内で化合物が意図した標的タンパク質に結合していることを確認することは、創薬研究や化学プローブ開発において重要なステップです。NanoLuc®ルシフェラーゼは、NanoBRET®ターゲットエンゲージメントアッセイプラットフォームの基盤となる酵素であり、バイオルミネッセンス共鳴エネルギー移動(BRET)を利用して、生細胞内におけるターゲット占有率、化合物の親和性、レジデンスタイム(滞留時間)、および細胞透過性を定量的に測定します。

NanoBRET® ターゲットエンゲージメントとは
ターゲットエンゲージメントとは、生体内において化学化合物が標的タンパク質と相互作用(または結合)することを指します。ターゲットエンゲージメントアッセイは、ターゲットバリデーション、構造活性相関(SAR)の確立、作用機序(MOA)の確認など、創薬プロセスのさまざまな段階で必要とされます。
プロメガでは、NanoBRET®ターゲットエンゲージメントアッセイと呼ばれる革新的なライブセル結合アッセイを開発しました。このアッセイは、バイオルミネッセンス共鳴エネルギー移動(BRET)と呼ばれるエネルギー移動技術を用いて、生細胞内で標的タンパク質と低分子化合物の結合を測定します。このエネルギー移動は、2つの要素に基づいています。このエネルギー移動は、NanoLuc® ルシフェラーゼ と融合した標的タンパク質の細胞内発現と、標的タンパク質に可逆的に結合する細胞透過性の蛍光NanoBRET®トレーサーという2つの要素に基づいています。

NanoBRET® テクノロジーの概要と ターゲットエンゲージメントアッセイの用途
NanoBRET® TE Cellular Assay で評価できる化合物の特性:
- 親和性と占有率:標的タンパク質に対する化合物の結合の強さと結合量の定量
- 選択制:類縁タンパク質との細胞内結合の比較評価
- 細胞透過性:化合物が細胞内に取り込まれる能力の算出
- レジデンスタイム(滞留時間):化合物が標的タンパク質に結合している時間の評価
実験開始オプション:
- 主要な創薬ターゲット用に最適化済みの NanoBRET® TE アッセイキット:
- 340 以上のキナーゼターゲット
- CRBN および VHL E3 リガーゼ
- 15種の RAS ダイマー (ホットスポット変異を含む)
- 5種の RAF ダイマー(プロモーター&ホモダイマーを含む)
- 9種以上の HDAC および BRD
- 10種以上の PARP
- NLRP3 インフラマソーム
- NanoBRET® 590 Dyes を利用した化学プローブまたはDELヒットからの新規トレーサーの合成
- Promega Services Team(アッセイ受託サービス)が化合物プロファイリングまたは新しいアッセイ開発をサポート
NanoBRET® TE アッセイのしくみ

標的タンパク質は、NanoLuc®ルシフェラーゼとの融合タンパク質として発現させます。そこに、標的タンパク質に可逆的に結合する細胞透過性の蛍光NanoBRET®トレーサーを添加します。ライブセル内で蛍光トレーサーが標的-NanoLuc®融合タンパク質に結合すると、NanoLuc®ルシフェラーゼとの近接により、BRETシグナルが発生します。テスト化合物が標的タンパク質に結合する場合、トレーサーと競合することでNanoBRET®シグナルが減少します。
親和性と占有率の定量
他の細胞内ターゲットエンゲージメントアッセイとは異なり、NanoBRET® TEアッセイは、単なるポテンシー評価にとどまらず、細胞内での化合物の親和性(または見かけのKi)を定量的に評価することができます。定量的な親和性測定は、NanoBRET®トレーサーの解離定数(Kd)以下、または同等の濃度で実験を行うことで実現されます。プロメガが開発した各標的特異的NanoBRET® TEアッセイには、細胞内でのNanoBRET®トレーサーの見かけの親和性および推奨トレーサー濃度が付属しています。
また、NanoBRET® TEは占有率(fractional occupancy)の定量にも対応しています。適切な実験コントロールを用いることで、BRET比は占有率に変換可能です。占有率を活用することで、キナーゼなどの類似した標的群における化合物の選択性を定量的に評価することができます。
ポスター「Cellular Kinase Assays that Deliver Quantitative Compound Affinity, Occupancy, and Selectivity in Live Cells using NanoBRET」では、NanoBRET® TEキナーゼアッセイを用いた定量化の方法とサポートデータの詳細について詳しく解説しています。
ポスターをダウンロードする
タンパク質複合体におけるターゲットエンゲージメント
NanoBRET® TEアッセイは、タンパク質複合体内における標的タンパク質への化合物の結合も定量的に評価することができます。このアプリケーションの初期の実装では、標的タンパク質とその結合パートナーを共発現させ、パートナーを過剰発現させることで、標的 - パートナー間の結合に特異的なバイアスのかかったシグナルを取得します。このアプローチの例として、サイクリン依存性キナーゼ(CDK)を対象としたNanoBRET® TEアッセイがあります。この場合、CDKとその共役パートナーであるサイクリンタンパク質を共発現させて評価を行います。
最新のバージョンでは、NanoBiT®システムがNanoBRET® TEアッセイに組み込まれており、BRETシグナルの発生が標的タンパク質と結合パートナーとの複合体形成に依存するように設計されています。このアプローチは、RASタンパク質およびRAFダイマーを対象としたNanoBRET® TEアッセイで使用されており、多量体複合体内でのターゲットエンゲージメントの評価を可能にします。NanoBRET® TE細胞内RAFダイマーアッセイを用いてRAFダイマー阻害剤のプロファイリングを行ったところ、形成されるCRAFダイマーの種類によって、CRAFに対する化合物の親和性が異なることが観察されました(詳細は製品ページをご覧ください)。
A.
B.
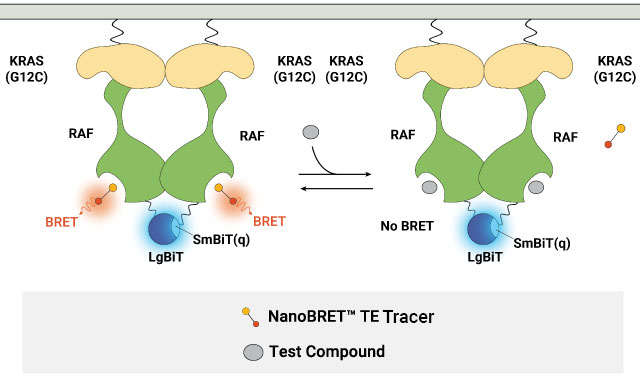
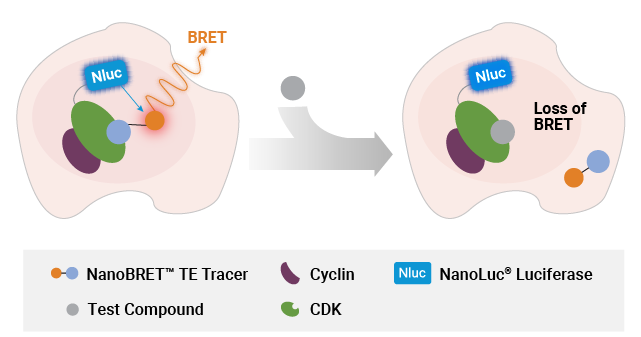
NanoBRET® TEアッセイによるタンパク質複合体における化合物結合の測定 A) CDKを対象としたNanoBRET® TEアッセイの原理図。CDK-NanoLuc®融合タンパク質とサイクリンパートナーを共発現させることで、CDK–サイクリン複合体の形成を促進する。 B) NanoBRET® TE Intracellular RAF Dimer Assayの模式図。RAFタンパク質にLgBiTまたはSmBiT(q)をタグ付けすることで、BRETシグナルがRAFダイマー複合体に特異的となるよう設計されている。
セルベースでの選択性プロファイリング
NanoBRET® TEアッセイの大きな特長のひとつは、生細胞内で化合物が複数の類縁タンパク質や変異体に対してどれだけ選択的に結合するかを、定量的に評価できる点です。これは、NanoBRET® TEアッセイが、生細胞内での化合物の占有率および親和性を複数のターゲットに対して同時に測定できるためです(詳細は上記をご参照ください)。この機能の一例として、NanoBRET® TE Intracellular RAS Assay では、RASリガンドに対する15種類のKRASおよびHRAS変異体それぞれでの細胞内親和性を評価しています。
100種類以上の標的に対する選択性プロファイリングを行う場合、単一濃度の化合物で各ターゲットの占有率を一括して測定できるNanoBRET® TEアッセイの能力が重要となります。このような大規模プロファイリングの例として、NanoBRET® TE K192 Kinase Selectivity System があります。このシステムには、キナーゼファミリー全体を幅広く代表する192種類のキナーゼが含まれており、各キナーゼにおける細胞内占有率を化合物ごとに測定できます。このシステムを使用することで、生化学的アプローチと比較して、細胞内での化合物の特異性が向上していることがよく観察されます。 また、CDKに特化した選択性プロファイリングには、NanoBRET® TE CDK Selectivity Systems をご利用いただけます。
プロファイリングを委託したい方へ
プロメガのTailored R&D Solutionsチームでは、NanoBRET® TEアッセイ(K192パネルまたはそれ以上のキナーゼパネルを含む)を用いた、化合物のターゲットプロファイリングサービスを提供しています。
A.

B.
NanoBRET® TE Cellular
Crizotinib, 16 hits
Biochemical
Crizotinib, 49 hits
NanoBRET® TEアッセイによる生細胞での選択性プロファイリング A) RAS阻害剤MRTX1133の選択性プロファイル例。KRASおよびその変異体には広く結合するが、HRAS変異体に対する親和性は低下している。 B) Crizotinib(1µM)を用いたターゲット占有率の比較。生細胞での NanoBRET® TE K192 Kinase Selectivity System と、セルフリーの生化学的アプローチによる結果を比較した。NanoBRET®を用いた評価では、細胞内での選択性スペクトルが向上していることが示された。
細胞内化合物到達性の評価
NanoBRET® TEアッセイは、化合物の細胞内到達性(intracellular availability)を評価するために使用できます。このパラメーターは、細胞膜透過性の指標として機能します。この評価は、NanoBRET® TEアッセイを2つのモード(ライブセルモード/膜透過処理済みセルモード)で実施することで行います。ライブセルモードでは、細胞膜がそのまま保持されており、化合物が標的にアクセスするのを阻害する可能性がある状態で見かけの細胞内親和性を測定します。一方、膜透過処理済みセルモードでは、細胞膜によるバリアが除去されており、化合物と標的の本来の親和性(固有親和性)を測定できます。この2つのモードで得られた親和性データを比較することで、細胞内到達性を定量的に計算することができます。
化合物間で細胞内到達性を比較できるように、膜透過性を有する標準化合物がコントロールとして使用され、正規化が行われます。これにより、「Availability Index(AI)」と呼ばれるパラメーターを計算することができ、複数の化合物間で相対的な細胞内到達性を比較することが可能になります。AI値が小さいほど、その化合物は細胞内に到達しやすいことを示します。化合物間での細胞内到達性の比較は、透過性に関わる物理化学的特性に基づいて候補化合物の優先順位を付ける手段として有用です。この評価は、PROTACs(高分子量化合物)のような細胞透過性が課題となる薬剤候補の開発において、特に重要な役割を果たします。

ポスター 「NanoBRET as a Live Cell Method to Evaluate PROTAC Affinity & Intra Intra Availability for E3 Ligases」では、NanoBRET® TE E3 Ligase Assay を例として用い、細胞内到達性の評価方法について詳しく解説しています。
レジデンスタイムの評価
NanoBRET®ターゲットエンゲージメントアッセイは、生細胞内で化合物のレジデンスタイム(滞留時間)を評価できるユニークな技術です。この評価では、標的タンパク質とNanoLuc®ルシフェラーゼの融合タンパク質を発現した細胞を使用し、ほぼ飽和濃度の化合物で平衡化させます。次に、未結合の化合物を除去し、細胞にほぼ飽和濃度のNanoBRET®トレーサーを添加します。この後、トレーサーの結合過程をリアルタイムで追跡します。標的タンパク質からの解離速度が遅い化合物は、トレーサーとの結合を妨げるため、BRETシグナルの発生が遅延します。このように、NanoBRET®トレーサーの高速結合特性と、NanoLuc®ルシフェラーゼの長いシグナル半減期により、生細胞内での結合速度および薬物のレジデンスタイムをリアルタイムでモニタリングすることが可能です。
アストラゼネカの研究者がNanoBRET® TEアッセイを用いて、化合物のレジデンスタイム(滞留時間)を測定し、ターゲット選択性に関わる新たな結合速度(キネティクス)の要素を明らかにした事例をご覧いただけます。
A.

B.

C.

NanoBRET®テクノロジーによる化合物のレジデンスタイム測定 A) ワークフローの概要 B) HDAC阻害剤の表現型ポテンシー。HDAC阻害剤で48時間処理すると、HeLa細胞において細胞内ATP量の減少を指標とした抗増殖効果が観察される。 C) レジデンスタイム解析により、FK228がHDAC1から非常にゆっくりと解離することが明らかとなり、FK228による長時間持続する表現型効果の説明となる可能性が示唆された。
独自のターゲットエンゲージメントアッセイを設計できます
NanoBRET®ターゲットエンゲージメントテクノロジーは、キナーゼ、HDAC、ブロモドメイン、GPCRなど、さまざまなクラスの標的タンパク質に適用可能です。ご興味のあるターゲットに対応したNanoBRET® TEアッセイが存在しない場合は、ご自身で開発することも可能です!NanoBRET® TEアッセイの開発は、以下の3つのステージで構成されます。
- 標的タンパク質に結合可能な蛍光トレーサー候補を合成します。NanoBRET® 590蛍光色素は、新規NanoBRET®トレーサーの作製に最適です。
- NanoLuc®ルシフェラーゼと標的タンパク質を融合させた発現ベクターを作製します。使用するベクターは、Flexi®ベクターシステム対応ベクターまたはマルチクローニングサイトを有するベクターを有するベクターのいずれかから選択できます。
- NanoBRET® TEアッセイにおけるトレーサー候補の性能を評価します。対象の標的が細胞内タンパク質である場合は、Intracellular TE Nano-Glo® Substrate/Inhibitor が必要です。本製品に含まれるコンポーネントにより、測定されるBRETシグナルが細胞内相互作用に由来することを保証します。
さらに詳しくは、NanoBRET® 590 Dye の製品ページをご覧ください。

関連資料
レジデンスタイムと標的結合の定量評価
このウェビナーでは、革新的なBRETアッセイを用いて、生細胞におけるターゲットエンゲージメントおよびレジデンスタイムを評価する方法をご紹介します。
ライブセルでのキナーゼターゲットエンゲージメントの評価
このウェビナーでは、キナーゼに対するターゲットエンゲージメントを生細胞で評価する方法について解説します。
ライブセルで明らかになった、CDK阻害剤の意外な選択性プロファイル
このブログ記事では、一部のキナーゼ阻害剤を、あまり研究されていないCDKファミリーメンバーに対する選択的な化学プローブとして再活用するための研究について紹介しています。