RAS パスウェイ 創薬
RASはヒトのがんにおいて最も頻繁に変異する癌遺伝子であり、KRAS は RAS ファミリーの中で最も頻繁に変異するサブタイプとして知られています。 肺がん、膵臓がん、大腸がんの多くは、KRASの変異によって引き起こされます。 最近、KRAS(G12C)特異的な共有結合阻害剤が発見されるまで、KRASは治療不可能なターゲットと考えられていました。
プロメガは、RAS 創薬を促進するためのいくつかのアッセイと技術を提供しています。これらのアッセイでは、パスウェイを構成するタンパク質への化合物の結合を測定し、タンパク質:タンパク質相互作用、タンパク質レベル、そして最終的にはERKの活性化に対する影響を評価することができます。
RAS経路の創薬に関する詳細な情報にご興味をお持ちですか?

Learn how Target Engagement Assays are used to study the RAS pathway in this poster: Comprehensive TE assays for the RAS pathway and its proximal effectors including SHP2
GTP が結合した活性化 Ras は RAF を活性化し、次いで MEK をリン酸化・活性化し、さらに ERK をリン酸化・活性化させます。
- RAS: KRAS、HRAS、NRAS を含む小型 GTPaseファミリー
- RAF: c-Raf、B-Raf、A-Raf からなるセリン/スレオニンキナーゼファミリー
- MEK: マイトジェン活性化プロテインキナーゼキナーゼ(MAPK/ERKキナーゼ)の一種
- ERK: 細胞外シグナル制御キナーゼファミリーで、マイトジェン活性化プロテインキナーゼ(MAPK)としても知られ、約85%の配列相同性を有するERK1 と ERK2 が存在

RAS-RAF-MEK-ERK パスウェイの概要
ターゲットエンゲージメント
NanoBRET™ Target Engagement Assay を利用すれば以下が可能になります:
- 生細胞内で化合物の親和性(タンパク質にどれだけ強く結合するか)と標的タンパク質の占有率(タンパク質にどれだけ化合物が結合するか)を定量化。
- 生理的条件下で、化合物が標的タンパク質に結合する時間(滞留時間)を評価。
- シンプルなマルチウェルアッセイで、研究スループットのニーズに合わせてスケールアップ可能。
- 低エラー率、高再現性で高品質なデータを生成。
- Ready-to-Use アッセイを利用すればすぐに実験可能。

NanoBRET™ Target Engagement Assay の原理
Learn more about NanoBRET® Target Engagement
Measure TE on Intracellular RAS Complexes
The NanoBRET® TE Intracellular RAS Assay measures intracellular compound binding to RAS proteins with ready-to-use assays for quantify compound affinity and fractional occupancy for multiple RAS variants, including KRAS, HRAS and related hot-spot mutants. Utilizing NanoLuc® Binary Technology (NanoBiT) complementation to create the energy donor enables the measurement of cellular target engagement on multimeric RAS complexes to more accurately reflect RAS biology. Measure engagement for individual RAS complexes or profile compound selectivity across RAS variants.


Pan-KRAS NanoBRET™ ターゲットエンゲージメントアッセイ. IC50 値は、生細胞(パネルA)および細胞溶解液(パネルB)において試験化合物について測定
プロメガの RAS NanoBRET™ TE Assay のさらに詳細はこちら
注目の論文
Nature Chemical Biology 誌に掲載されたこの論文では、KRAS低分子阻害剤の可逆的結合性を調べ、どのホットスポット変異体が細胞内におけるスイッチIIポケット(SII-P)への結合性に対して脆弱であるかを評価しました。その結果、多くのKRASホットスポット変異体のSII-Pは、非共有結合性リガンドを用いてアクセスできることがわかりました。この結果は、SII-PがKRASの特異的な薬物結合部位であることを強調し、RAS駆動型がんの新たな治療機会を明らかにするものです。

特定のタンパク質間相互作用におけるTEの条件付き定量化
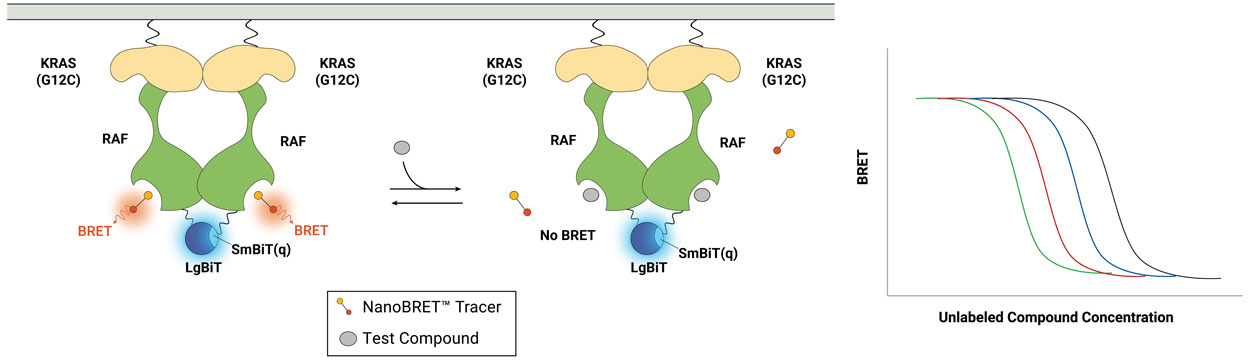

BRAF, CRAF or ARAFのプロトマー特異的アッセイについては CRAお問合せください。
注目の論文
RAS-RAF 複合体中のRAFプロトマーを標的とするRAFダイマー阻害剤は、RAS駆動型がんの治療に有望です。この論文では、活性型 RAS-RAF 複合体における薬剤の占有率を定量化し、阻害剤の評価に役立てる新しい方法を紹介しています。臨床第II相RAF阻害剤は主にARAFプロトマーに関与し、変異RAS細胞株におけるMAPKシグナル伝達に影響を与え、ARAFの重要な役割を明らかにしました。

RAF、MEK、ERKを 含むキナーゼターゲットエンゲージメントアッセイの全リストは、選択リスト をご覧ください。
RAS 経路の研究にターゲットエンゲージメントアッセイがどのように使用されているかについては、このポスターをダウンロードしてください:
Comprehensive TE assays for the RAS pathway and its proximal effectors including SHP2

HiBiT:LgBiTの相補性を利用した細胞内のタンパク質分解実験の模式図
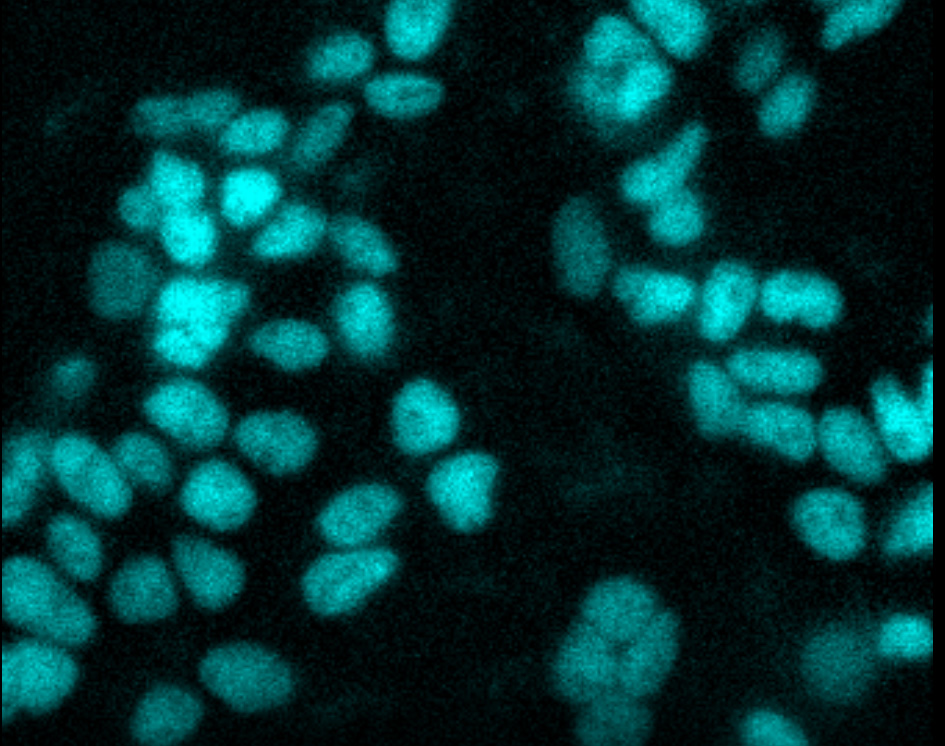
タイムラプスライブセルイメージング. CRISPR-HiBiT BRD4 細胞をBET ブロモドメイン分解剤であるMZ1で処理した。BRD4の均一な消失が2時間にわたって観察された。イメージングには、Olympus LV200 Systemを使用した。
タンパク質分解実験への HiBiT の利用
HiBiT は内在性タンパク質の分解を研究するためのタグとして汎用されています。HiBiTは小さな11アミノ酸のペプチドで、LgBiTと呼ばれる大きなサブユニットに高い親和性で結合します。結合した複合体は高いルシフェラーゼ活性を持ち、添加した基質の存在下で明るい発光シグナルを生じます。HiBiTタグはサイズが小さいため、分子クローニングのステップを必要とせず、大きなタグと比較して高いノックイン効率が得られ、CRISPR/Cas9 ゲノム編集ワークフローに適しています。
分解を誘発する化合物を添加すると発光シグナルが消失するため、定量性が高く、リアルタイムで分解効率を測定することが可能です。細胞の用量反応曲線が得られ、24時間から48時間の時間枠でモニターできるため、分解速度、Dmax、DC50値、タンパク質回収率を正確に決定することができます。このアプローチにより、一連の様々なパラメータに対する分解効率の迅速なランク付けが可能となり、このアッセイはハイスループット・スクリーニングにも適しています。
A.

B.

PROTAC処理後の内在性 HiBiT-KRasG12Cのライブセル分解キネティクス. パネル A. MIA-PaCa2細胞株のN末端内在性 KRasG12C 遺伝子座にCRISPR/Cas9を介してHiBiTを挿入した。LgBiTの発現後、 Nano-Glo® Endurazine™ Substrate を含むCO2非依存性培地で、VHLベースのKRasG12C PROTAC、LC-2を用いて用量反応動態分解実験を実施した。フラクショナルRLUは、DMSOコントロールに対する相対値でプロットされています。パネルB. 親阻害剤 MRTX849を用いたMIA-Paca2 細胞におけるHiBiT-KRasG12Cの同様の生細胞発光実験では同じ用量反応処理でKRasG12Cの消失は見られなかった。
Need to quantify protein levels in disease-relevant cellular models?
We provide ready-to-use HiBiT knock-in cell lines and pools, including WT and mutants for KRAS, NRAS, ARAF, BRAF and RAF1.| KI Cell Line | Background |
|---|---|
| HiBiT-KRAS(G12C) | MIA PaCa-2 |
| HiBiT-KRAS(G12D) | AsPc-1 |
| HiBiT-KRAS(G12D) | SW1990 |
| HiBiT-KRAS(G12D) | HEK293 |
| HiBiT-KRAS(G12S) | A549 |
| HiBiT-KRAS(G12V) | HEK293 |
| HiBiT-KRAS(G12V) | SW620 |
| HiBiT-KRAS(G13D) | NCI-H647 |
| HiBiT-KRAS(WT) | HEK293 |
| HiBiT-KRAS(WT) | NCl-H1299 |
| HiBiT-NRAS(Q61R) | SW1271 |
| HiBiT-NRAS(WT) | HEK293 |
| HiBiT-ARAF | A549 |
| HiBiT-BRAF | A549 |
| HiBiT-BRAF(V600E) | A375 |
| RAF1-HiBiT | A549 |
| RAF1-HiBiT | Hs766T |
| RAF1-HiBiT | PANC 08.13 |
タンパク質間相互作用
NanoBRET™テクノロジーは、生きた細胞環境におけるタンパク質間相互作用(PPI)を高感度かつ再現性よく検出することができます。低レベルで発現する完全長タンパク質を使用することで、真の細胞生理を反映したPPI モニタリングとスクリーニング研究が可能になります。明るく青くシフトしたドナーシグナルと赤くシフトしたアクセプターは、従来のBRETアッセイと比較して、最適なスペクトルのオーバーラップ、シグナルの増加、バックグラウンドの低下を生み出します。

NanoBRET™ PPI アッセイの測定原理
以下の論文では、NanoBRET™技術の機能についての詳細や、サンプルデータをご覧いただけます:
Machleidt, T. et al. (2015) NanoBRET—A novel BRET platform for the analysis of protein–protein interactions. ACS Chem. Biol. 10(8), 1797–1804.
NanoBRET™ PPI がRAS 経路の研究にどのように使用されているか、このポスターでご覧ください。
A.

B.

シグナル経路におけるタンパク質相互作用の阻害および誘導を研究するための、RASおよびRAFファミリーメンバーにわたるNanoBRET™アッセイ. BI-2852阻害剤を用いたRAS:RAFアッセイ(パネルA)、GDC0879によるRAF 二量体化誘導を示すRAFアッセイ(パネルB)。
A.

B.

KRAS WT : SOS1cat ドメイン相互作用の阻害. SOS1触媒ドメインは、BI-3406とBAY-293の用量反応処理によりKRAS WTからの解離を示す。
NanoLuc® バイナリーテクノロジー(NanoBiT)は、NanoLuc® ルシフェラーゼをベースにした2サブユニットシステムで、生細胞内のタンパク質間相互作用検出に応用することができます。この短いビデオでは、この技術がどのように機能するかを説明しています。

NanoBiT® PPIアッセイの原理
RAS経路に関与するタンパク質間相互作用を研究するためのNanoBiT®テクノロジーの使用例について詳しくは、野生型および変異型KRASとCRAFまたはBRAFとのペアのデータを示すこのスライドデッキをダウンロードしてください。
NanoBiT®テクノロジーの起源については、こちらの論文でご覧ください。Dixon, A. S. et al. (2016). NanoLuc Complementation Reporter Optimized for Accurate Measurement of Protein Interactions in Cells. ACS Chemical Biology. p. 400-408



KRAS 4B 野生型および変異体とRAFアイソフォームの相互作用をモニターするNanoBiT®アッセイ. KRAS 4BとCRAF RBDドメイン(パネルA);KRAS 4Bと完全長CRAF(パネルB);KRAS 4Bと完全長BRAF(パネルC)。

EGF処理後の血清飢餓 HeLa細胞 における KRAS 4B(WT):CRAF(完全長)相互作用のリアルタイムモニタリング
NanoLuc®、HaloTag®、NanoBiT®、BiBRETベクターをご用意しておりますので、PPIアッセイを開始する際にお役立てください。生細胞で RASパスウェイ相互作用を調べるための利用可能なアッセイのリストを参照ください。
タグ付加タンパク質の PPI 検出

Lumit™ タンパク質間相互作用 (PPI) イムノアッセイでは、ストレプトアビジンおよび汎用されるタグに対する抗体をLgBiTとSmBiTで標識しています。異なるタグを持つ2つのタンパク質が結合すると、対応するSmBiTおよびLgBiTコンジュゲート抗体を用いて相互作用を検出することができます。


KRAS(G12C)/RBD-cRAF Interaction with AMG510

Lumit™ KRAS-cRAF アッセイは、KRAS変異体のパネルに対する低分子阻害剤の特異性をテストするために使用可能
Kinetics of KRAS(G12C)/RBD-cRAF interaction

KRASの活性化サイクルを in vitroで再構成し、SOS1を介したGDP/GTP交換の反映として、低分子阻害剤存在下でKRAS/CRAF結合の動態をモニターすることが可能。
詳しくは、アプリケーションノートまたはLumit™ Immunoassay Cellular Systemの製品ページをご覧ください。
リン酸化 ERK

Lumit™ Immunoassay Cellular System の測定原理

Lumit™ p-ERKイムノアッセイを用いたKRASの研究については、以下の論文で詳しく解説しています:
Swiatnicki, M. et al. (2022) Profiling oncogenic KRAS mutant drugs with a cell-based Lumit p-ERK immunoassay. SLAS Discovery. p 249-247.

RAS 変異体阻害剤. Lumit™アッセイにより、個々の変異型 KRAS 阻害剤の細胞内p-ERK阻害プロファイルが示された。MCF-7(WT)、SW620(G12V変異体)、Mia-PaCa-2(G12C変異体)、AsPC-1(G12D変異体)で様々な変異型 KRAS 阻害剤の滴定を実施し、KRAS 阻害を検出する指標としてLumit™ p-ERG が使われました。パネルA-C. KRAS G12C化合物の高い選択性がp-ERK Lumit™アッセイで示され、Mia-PaCa-2細胞は完全に阻害され、KRAS WT、G12D、G12V細胞は全く阻害されないことがわかります。パネルD. Lumit™アッセイにより、MRTX-1133はKRAS G12Dに対して非常に選択的であり、高いIC50ではKRAS G12CおよびG12Vに対して若干の交差反応性を示した。
詳しくは、アプリケーションノートまたはLumit™ Immunoassay Cellular Systemの製品ページをご覧ください。
GTPase
プロファイリングサービス
プロメガの カスタムアッセイサービス は、お客様の創薬および薬剤開発のワークフローを加速するのに役立ちます。これらの包括的なサービスは、感度が高く、ハイスループットで、生物学的に適切な結果を得るための当社の技術に基づいて構築されています。詳細については、 Tailored R&D Solutions チームにお問い合わせください。
- 生細胞 ターゲットエンゲージメント
- CRISPR-HiBiT 細胞株
- タンパク質間相互作用
- Lumit™ イムノアッセイ
- その他