細胞治療のための有効性および機能測定
Potency有効性および機能アッセイは細胞治療の開発において不可欠で、細胞製品の治療効果や一貫性に関する重要な情報を提供します。有効性アッセイは細胞の生物学的活性を測定し、目的とする治療効果を達成しているかどうかを確認できます。一方で、機能アッセイは、分化能力や因子の分泌、疾患細胞の標的化能力などの細胞が有する特定の機能を評価可能です。これらのアッセイは、細胞治療の有効性や安全性、信頼性を検証する上で不可欠です。細胞治療開発の過程において、細胞の有効性や機能性についての疑問点と解決方法をご案内します。
このウェビナーではCAR-T細胞の有効性評価のための新たな標的細胞殺傷(TCK)ベースのアプローチについて紹介しています。
細胞が期待されるタンパク質またはサイトカインを産生しているかを調べる
Lumit® Technology は細胞が期待されるタンパク質を産生しているか、または目的のサイトカインを分泌しているかを検出するための、高感度な発光ベースの検出方法です。この手法は、シンプルで迅速な「洗浄不要」プロトコルにより、ELISAに代わる高速かつ信頼性の高いアッセイを実現しています。また、細胞培養中の生体分子を直接検出・定量可能であり、細胞機能やタンパク質発現のリアルタイムな観察を可能にします。これらのアッセイは細胞治療の機能性検証に特に有用であり、目的タンパク質やサイトカインの量を正確に測定することで、細胞が期待通りに機能していることを確認できます。
CAR-T細胞
Lumit® Cytokine Immunoassays は、CAR-T細胞やCAR-NK細胞のような活性化された遺伝子改変免疫細胞からのサイトカイン産生を検出するために特別に設計されています。これらのアッセイは細胞に直接使用できるため、一般的なエラーの原因となる培地の移し替え、希釈、洗浄ステップが不要です。また、広い直線範囲を持つため、Lumit® Cytokine Immunoassay は多くの細胞モデルで予想される濃度範囲をカバーできます。
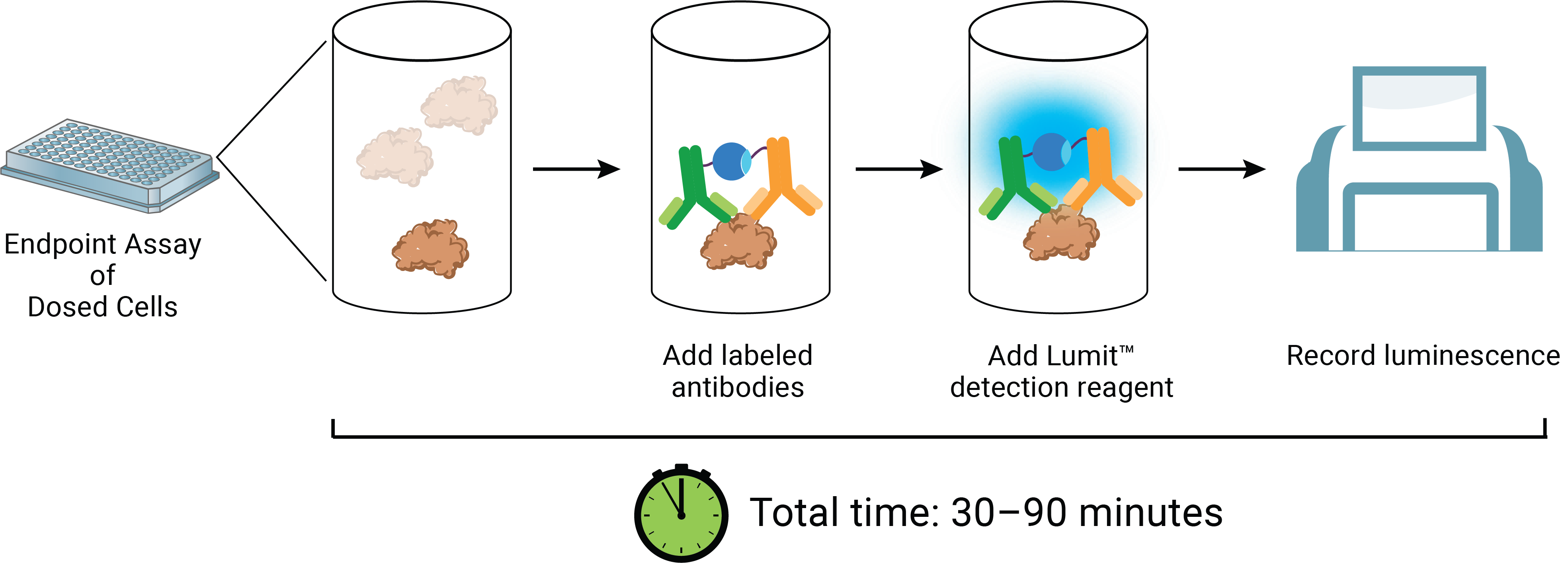

パネル(左):洗浄不要なLumit® Immunoassayワークフロー。パネル(右):高精度なCAR-T細胞のサイトカイン分泌測定。CAR-19レンチウイルスで形質導入したT 細胞を、異なるエフェクター対ターゲット(E:T)比でRamos標的細胞と混合し、24時間インキュベートしました。その後、Lumit® IFN-γ (Human) Immunoassayを用いてIFN-γの分泌量を定量しました。
iPSC由来細胞
誘導多能性幹細胞(iPSC)を利用した細胞治療は神経変性疾患(例:パーキンソン病)、心疾患、糖尿病、がんなど様々な疾患に対する有望な治療違法です。iPSCはニューロン、心筋細胞、インスリン産生細胞などの特定の細胞型へと分化させることが可能であり、それらを用いて損傷した組織や疾患組織を置換できます。機能アッセイは、iPSC由来細胞の機能性と品質を評価する上で重要であり、これらの細胞が自然な細胞を効果的に模倣し、必要な機能(例:iPSC由来膵β細胞によるインスリン分泌)を果たせるかを確認するために行われます。
Lumit® Insulin および Glucagon Immunoassays は、培養中の膵島細胞またはiPSC由来膵細胞から分泌されるインスリンやグルカゴンを測定するための生物発光を用いたELISAの代替法です。このアッセイは迅速で簡便、かつ洗浄不要のプロトコルを特長とし、膵島細胞からのホルモン分泌の定量に理想的なアッセイです。
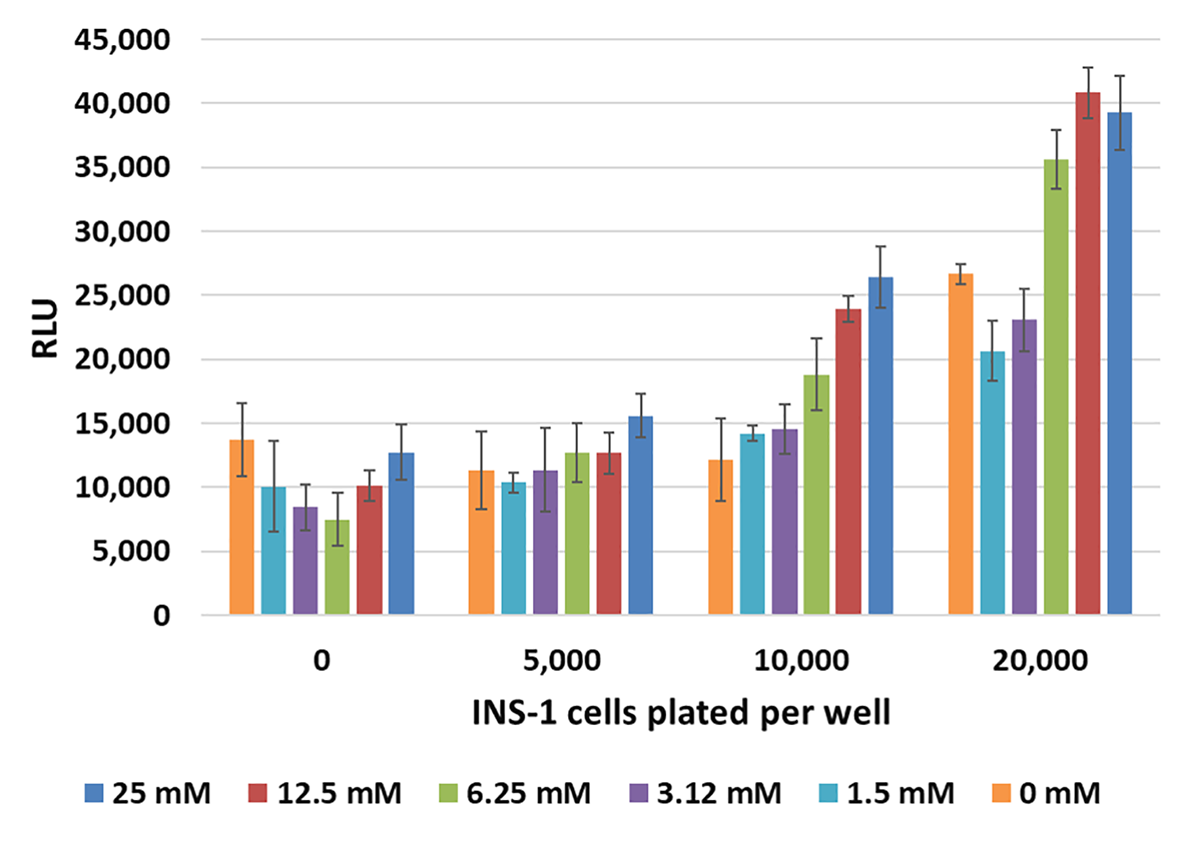
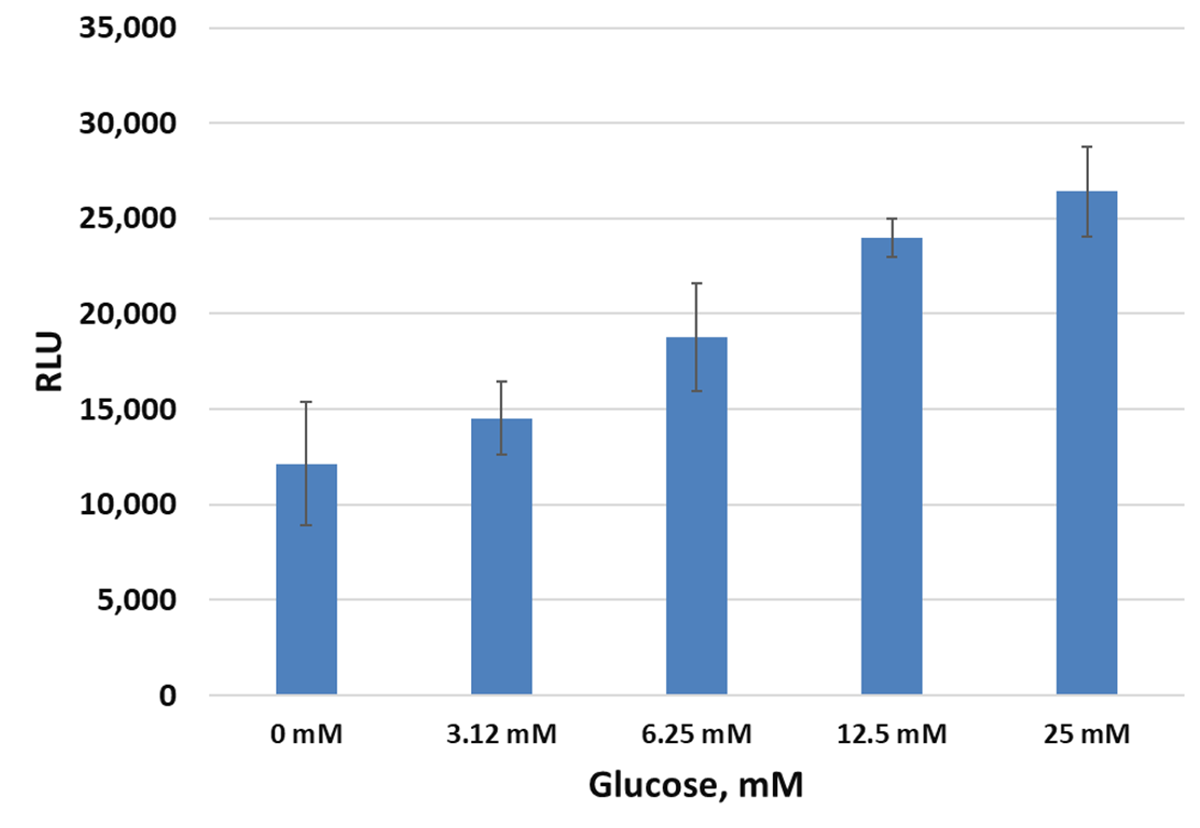
Lumit® Immunoassayを用いた細胞のグルコース刺激に対するインスリン分泌反応の測定 パネル(左): INS-1細胞を96wellプレートに異なる細胞数/wellで複数ウェル播種し、グルコース刺激によるインスリン分泌実験を実施しました。60分後に、10μl回収し、384wellプレートでLumit® Insulin Immunoassay を実施しました。エラーバーは±1 s.dを示しています。パネル(右):同一実験における10,000細胞/ウェルの条件で得られたデータを示しており、グルコース濃度の上昇に伴うインスリンの分泌増加がみられます。
ターゲットセルキリングにおけるCAR-T細胞の有効性評価
有効性アッセイは細胞治療が意図する生物学的な効果を特異的に測定できるように設計されているべきです。免疫細胞治療(e.g., CAR-T, TCR-T, TILs and CAR-NK)の場合は、ターゲットセルキリングアッセイは前臨床開発および製造プロセスにおいて、細胞の有効性、安全性、機能性に関する重要なデータを提供し、治療法を臨床応用向けて最適化する上で重要な要素です。
既存の多くの細胞生存性アッセイはターゲット細胞に特異的ではなく、治療効果を正確に測定する上で課題となっています。他の一般的なセルキリングアッセイは蛍光色素とフローサイトメトリーを用いており、処理工程が長く、ドナー間のぱらつきが大きく、取扱いに時間がかかり、感度が低くバックグラウンドが高いといった課題があります。また、解析も複雑で標準化されていません。
シグナル増加型アッセイ
作用機序(MOA)に基づいたHiBiT Target Cell Killing (TCK) Bioassay は簡便に実施でき、エフェクター細胞によるターゲットセルキリングを高感度かつ特異的に測定可能です。ホタルルシフェラーゼ発現腫瘍細胞が殺傷されることで発生する発光シグナルの減少を測定する従来の方法とは異なり、HiBiT TCK Bioassayはエフェクター免疫細胞による標的細胞の溶解により、明るい発光シグナルを生じます。


パネル(左):HiBiT TCK Bioassayの原理細胞障害性モノクロナール抗体(mAb)とエフェクター細胞をHiBiT融合タンパク質発現ターゲット細胞と共に培養します。標的細胞の殺傷が生じると、HiBiT融合タンパク質が放出され、細胞外のLgBiTと結合することで機能的なNanoBiT® Luciferase酵素を形成します。この発光はルミノメーターで測定可能です。パネル(右):HiBiT TCK Bioassayを使用したCAR-T細胞依存性細胞障害活性の測定。 H929 Cells (HT-HiBiT)は E:T比で示した比率でヒトBCMA CAR-T細胞に連続希釈して培養しました。4、24、48、または72時間の誘導後、Bio-Glo-NB™ TCK Reagentを添加し、GloMax® Discover Systemを用いて発光値を測定しました。※HTはHaloTagを表し、HiBiT tagの融合パートナーです。
シグナル減少型アッセイ
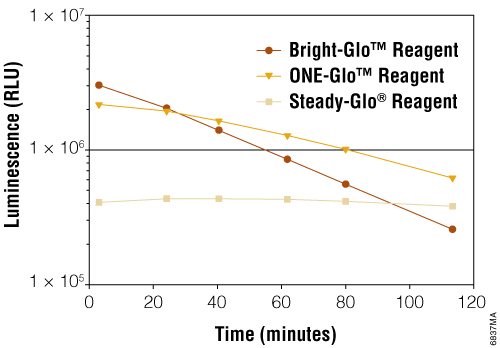
CAR-T細胞もしくはその他の免疫細胞依存の腫瘍細胞に対する細胞障害効果はホタルルシフェラーゼ等のルシフェラーゼを発現させた腫瘍細胞と免疫細胞の共培養によって評価されることも多くあります。Bright-Glo™ (Foukle et al., 2024; Kim et al., 2023; Rodriguez-Marquez et al., 2022) および One-Glo™ Luciferase Assay Systems (Panowski et al, 2020) は哺乳類細胞におけるホタルルシフェラーゼレポーター遺伝子発現の検出するための高感度、堅牢、均一なアッセイです。腫瘍細胞の発光シグナルの減少はエフェクター免疫細胞細胞障害効果を示しています。
新規TCR/CARのスクリーニングおよびバリデーション方法
新規光源特異的T細胞受容体(TCR)またはCARの探索および開発の過程において、プロメガの生物発光ルシフェラーゼレポーターT細胞活性化バイオアッセイはTCRやCARの機能をモニタリングまたはバリデーションするために使用可能です(Nishimura et al., 2024; Uchibori et al., 2019; Jahan et al., 2023)。
CAR-T製造に用いられるレンチウイルスベクターでは、CAR-T細胞でのウイルスベクターのトランスジーン発現だけではなく、さらなる有効性評価も要求されます。プロメガの作用機序ベースのT細胞活性化バイオアッセイは、T細胞誘導レンチウイルスベクターに由来するCARとターゲット細胞の結合を測定し、ご自身のCAR-Tワークフローに適合する安定性指標を備えた定量可能な発光リードアウトを提供します。
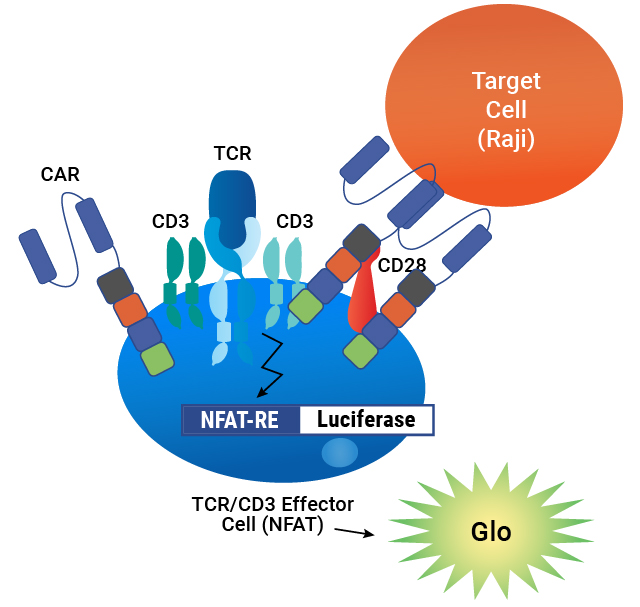
アッセイ原理 . CARは、NFAT-Luciferaseレポーターを含むTCR/CD3エフェクター細胞の表面に発現します。CARがターゲット細胞上の抗原と結合すると、シグナル伝達に比例して発光が誘導されます。

T細胞活性化バイオアッセイ(NFATおよびIL-2)は、それぞれ遺伝子改変された細胞株で構成されており、TCR/CD3エフェクター細胞 NFAT(パネルA)または IL-2(パネルB)を使用します。これらの細胞が、抗TCR/CD3刺激単独、または抗TCR/CD3と抗CD28の両刺激と結合すると、受容体を介したシグナル伝達が発光を誘導します。
Lentivirus Bioassay is Specific

CAR-19レンチウイルスを導入した細胞に対する応答特異性. TCR/CD3エフェクター細胞をCAR-19またはGFPレンチウイルスの連続希釈液で形質導入しました。48時間後、Raji ターゲット細胞(CD19+)を加え、6時間の誘導期間後に発光を検出ました。CAR-19レンチウイルスを導入したTCR/CD3エフェクター細胞のみが、Raji ターゲット細胞に対する反応を示しました。

抗原ノックアウトにより提示されるアッセイ特異性. TCR/CD3エフェクター細胞をCAR-19 レンチウイルスの連続希釈液で形質導入しました。48時間後、Raji ターゲット細胞またはCD19ノックアウトRaji ターゲット細胞を加え、6時間の誘導期間後に発光を検出しました。ターゲット細胞に対する反応は抗原ノックアウトにより消失し、このアッセイの特異性が示されました。
Lentivirus Bioassay Is Stability Indicating

| Heat Treatment Time (hours) |
EC50 |
% Inhibition of Max |
|---|---|---|
| 0 |
0.81 | Reference |
| 2 |
1.0 |
26% |
| 6 |
2.4 |
18% |
| 24 | 2.5 |
47% |
| 48 | 5.0 |
67% |
CAR-19レンチウイルスの強制劣化サンプルは、37°Cで2〜48時間インキュベートすることで調製され、その後、TCR/CD3エフェクター細胞およびRaji標的細胞を用いて解析されました。 本アッセイは、熱処理によりレンチウイルスの有効性が低下することを示しており、EC50の上昇および最大応答の低下として測定されました。
これらのアッセイは内因性のTCRαβ鎖を発現しておらず、トランスジェニックTCRとのα鎖およびβ鎖のクロスペアリングを排除することで、アッセイウィンドウが向上しています。

T細胞活性化バイオアッセイ(TCRαβ-KO)の原理 トランスジェニックTCRを発現していないTCRαβ-KO細胞は、ペプチドやMHCによって活性化されることがなく、発光は低いままです。一方、TCRを発現するようにトランスフェクションまたはトランスダクションされたTCRαβ-KO細胞は、抗原提示細胞(APC)および認識抗原によって活性化され、TCRシグナル伝達経路により発光が誘導されます。


T Cell Activation Bioassay(TCRαβ-KO、CD4+)を用いて測定したトランスジェニック TCR の活性 パネルA:TCRαβ-KO(CD4+)細胞を陽性コントロール TCR プラスミドでトランスフェクトし(またはモックトランスフェク ト)、MHCII APC 細胞(HLA-DR+細胞)および濃度を増加させた陽性コントロールペプチドと共培養しました。パネルB:TCR を介した T 細胞活性化を、T Cell Activation Bioassay(内在性 TCR、CD4+)および T Cell Activation Bioassay(TCRαβ-KO、CD4+)を用いて測定しました。T Cell Activation Bioassay の細胞は、HLA-DR陽性細胞および増加する同族ペプチドと共培養しました。腫瘍細胞上の抗原と結合することにより改変T細胞が活性化されたことが発光によって示されました。このデータは、T Cell Activation Bioassay が、T細胞免疫療法に使用されるトランスジェニックTCRのスクリーニングに使用できることを示しています。
動物モデルにおける機能確認
In vivo生物発光イメージングは、生体内における細胞治療の経過や分布、有効性、あるいは潜在リスクをモニタリングするために広く利用されています。ルシフェラーゼレポーターは自己蛍光がないため、高いシグナル対バックグラウンド比と低い検出限界を実現し、組織細胞の高感度かつ非侵襲的なイメージングを可能にしています。
ホタルルシフェラーゼ(FLuc)とNanoLuc®ルシフェラーゼ(NLuc)は、それぞれの酵素が基質に対して交差反応を示さないため、二重イメージングの際に併用することができます。これらの生物発光レポーターを用いたマルチプレックス解析では、CAR-T細胞 (Su et al., 2020)とCAR-NK細胞(Shalaby et al., 2024)による腫瘍標的細胞の局在および殺傷の追跡が実証されています。
発光レポーターと基質
| レポーター | 基質 |
|---|---|
| Firefly luciferase (FLuc) | VivoGlo™ Luciferin, In Vivo Grade |
| NanoLuc (NLuc) | Nano-Glo® Fluorofurimazine In Vivo Substrate (FFz) |
| Renilla (RLuc) | ViviRen™ In Vivo Renilla Luciferase Substrate |
ご希望にぴったりなバイオアッセイが見つからない場合は...
私たちのテーラード R&D ソリューションチームがお客様のカスタムバイオアッセイの開発をお手伝いします。