肥満研究ソリューション
肥満のメカニズムを研究し、安全で効果的な治療法の開発を加速するための革新的なツールについて学びましょう。私たちは、GPCRシグナル伝達、エネルギー代謝、および炎症を測定するためのソリューションを提供しています。
研究の課題解決をサポートします。いつでもご相談ください!
肥満と新薬開発
肥満は、遺伝的、ホルモン的、および炎症性の要因によって影響を受ける多面的な代謝疾患です。新薬開発の取り組みは、食欲、エネルギー代謝、脂肪貯蔵を調節する主要な経路をターゲットにしており、GPCR、ホルモンシグナル伝達、炎症性サイトカイン、筋肉代謝に対する関心が高まっています。
代謝および炎症性バイオマーカー、機能的受容体アッセイ、およびミオスタチン阻害における最近の進歩は、次世代の肥満治療を形作っています。これらの複雑なメカニズムを理解することは、体重減少だけでなく、代謝健康および肥満関連の併存疾患に対処する効果的な治療法を開発するために重要です。
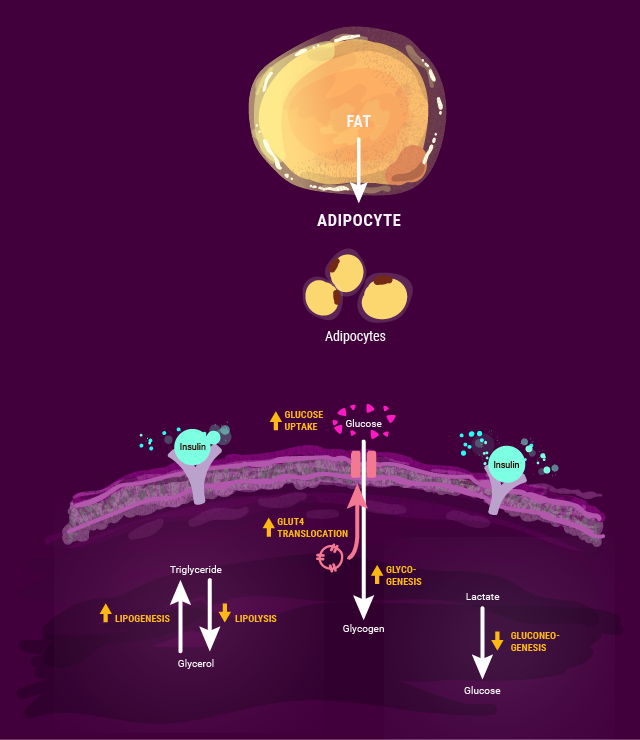
GPCRs
Gタンパク質共役受容体(GPCR)は、食欲調節、エネルギー消費、代謝恒常性などの重要な生理的プロセスを媒介するため、肥満において重要な役割を果たしています。GLP-1のようなホルモンのターゲットとして、GPCRは多くの肥満治療の中心となっています。
GPCR研究に役立つ包括的なツールをご覧ください。これには、リガンド結合、タンパク質間相互作用、cAMPシグナル伝達、受容体内在化、および遺伝子発現のアッセイが含まれます。
HiBiTを利用したアゴニスト誘導性GPCR内在化のモニタリング
CRISPR遺伝子編集を使用して、目的のGPCRに小さな発光性のペプチドタグ HiBiT をタグ付けすることで、アゴニスト結合後、受容体内在化は発光アッセイを通じてリアルタイムで定量化できます。受容体の動態およびシグナル伝達の変動の研究に役立つ、高感度でスケーラブルな方法を提供します。
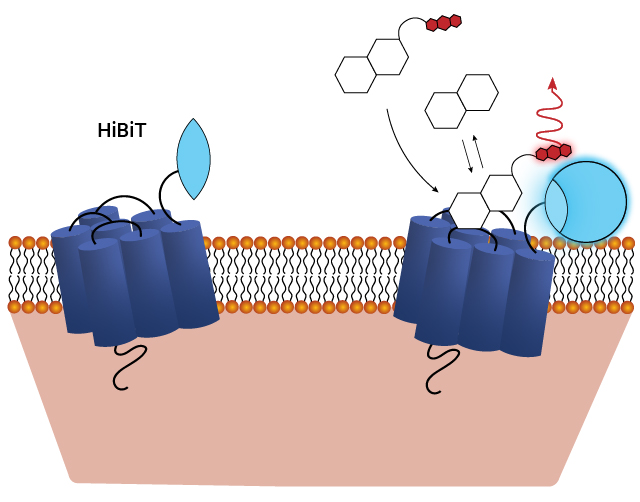
HiBiT/LgBiTレポーターを利用したリガンド誘導性GPCR内在化をモニターするアッセイの概略図 本資料で詳細をご覧ください。: The luminescent HiBiT peptide enables selective quantitation of G protein–coupled receptor ligand engagement and internalization in living cells.

Quantifying the affinity of GLP-1R ligands using the NanoBRET® TE assay and HiBiT-tagged GLP-1R. See details in this Application Note: Detection of GLP1R Target Engagement
Monitor Agonist-Induced GPCR Internalization with HiBiT
Tag your GPCR of interest with a small, luminescent HiBiT peptide via CRISPR gene editing. Upon agonist binding, receptor internalization can be quantified in real-time through a luminescence assay, offering a sensitive and scalable method to study receptor trafficking and signaling dynamics.
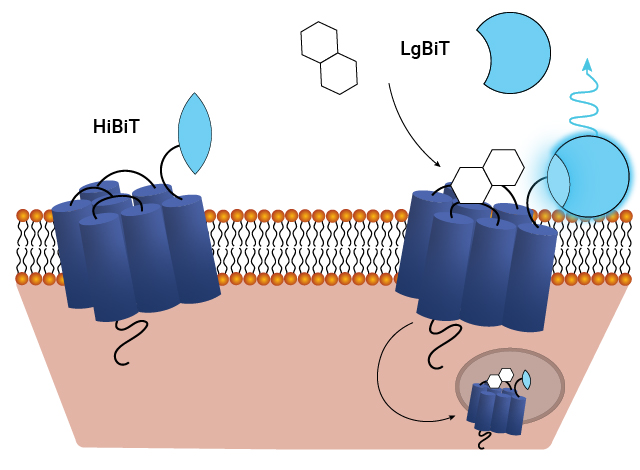
Schematic of assays utilizing the HiBiT/LgBiT reporter for monitoring ligand-induced GPCR internalization. See details in this publication: The luminescent HiBiT peptide enables selective quantitation of G protein-coupled receptor ligand engagement and internalization in living cells.
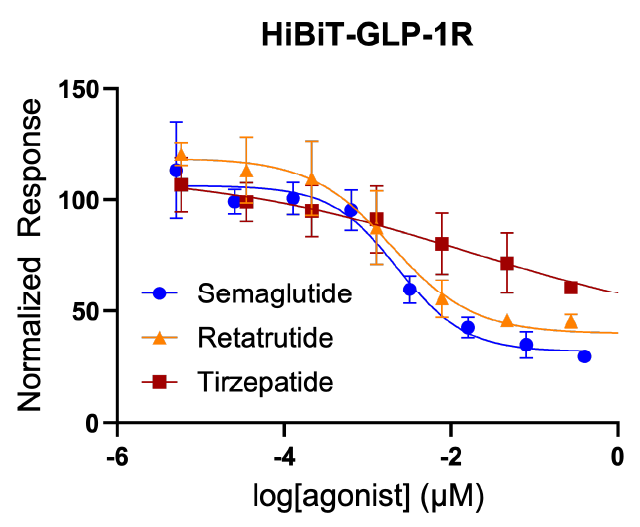
Measurement of agonist-induced internalization of HiBiT-tagged GLP-1R. See details in this poster: Advancing Therapeutic Strategies for Obesity: Innovative Bioluminescence Assays for Monitoring GPCR Dynamics
β-アレスチン結合のリアルタイム解析
NanoBiT® Technology は受容体とβ-アレスチンを補完的なルシフェラーゼ断片と融合させることで、GPCRへのβ-アレスチンの結合のリアルタイムモニタリングを可能にします。受容体の活性化とβ-アレスチンの結合により、断片が機能的なルシフェラーゼ酵素を再構成し、β-アレスチンの結合と直接相関する発光シグナルを発します。
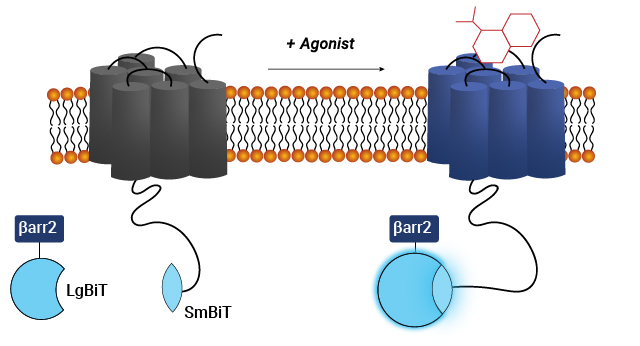
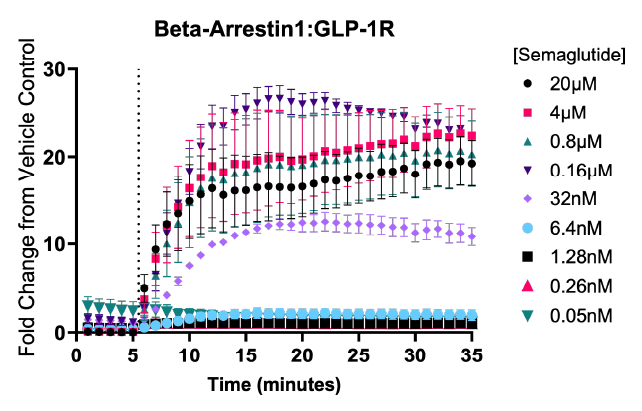
アゴニスト誘導性のβ-アレスチンとGLP-1Rの結合をリアルタイムでモニタリング 詳細はこちら: Advancing Therapeutic Strategies for Obesity: Innovative Bioluminescence Assays for Monitoring GPCR Dynamics
cAMP量のリアルタイムな変動を測定
弊社のcAMP assays は、アゴニスト誘導性の細胞内cAMP量の変動をモニタリングするための、高感度、ハイスループットなソリューションを提供し、GPCRシグナル伝達の動態を正確に特徴づけます。
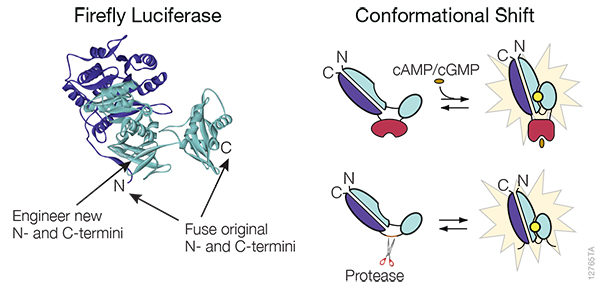
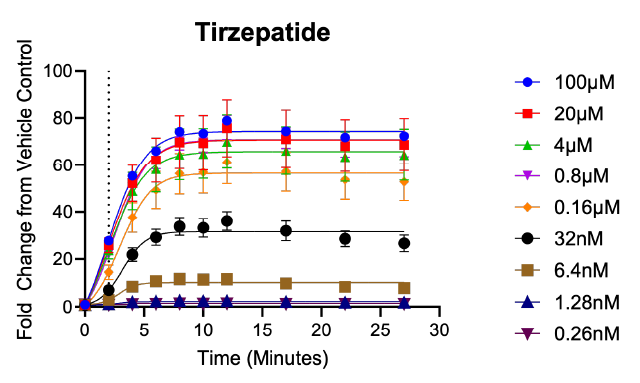
GloSensor™ technologyを使用したGLP-1Rアゴニスト誘導性のcAMP量変動のリアルタイムモニタリング 詳細はこちら: Advancing Therapeutic Strategies for Obesity: Innovative Bioluminescence Assays for Monitoring GPCR Dynamics
エネルギー代謝とその制御
エネルギー代謝は肥満研究の中心であり、グルコースおよび脂質の恒常性を調節するプロセスを含みます。これらの相互に関連する経路を理解することは、代謝バランスを回復する治療標的を特定するために重要です。インスリン分泌、グルコース取り込み、脂質代謝などの主要なバイオマーカーを測定するアッセイは、エネルギー調節の複雑さを理解し、より効果的な肥満治療を開発するのに役立ちます。
高感度な代謝測定のための生物発光アッセイの豊富なラインナップをご覧ください。
インスリン / グルカゴンの測定
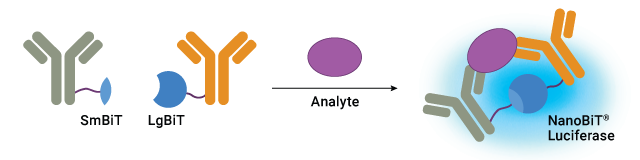
ホルモン量の測定は、肥満におけるグルコースおよび脂質恒常性の調節不全を理解するために不可欠です。インスリン抵抗性はこの疾患の特徴です。インスリンやグルカゴンを測定可能なLumit® Immunoassaysは、洗浄不要の簡便な発光アッセイのため、肥満研究におけるホルモン分泌やシグナル伝達の正確かつ迅速な分析を可能にします。

グルコースの測定
グルコース代謝は肥満研究の中心的な役割を果たしており、グルコース量の制御不全や取り込み障害がインスリン抵抗性および代謝機能障害の主な原因です。グルコースの検知や取り込みメカニズムを理解することは、肥満に関連した症状や潜在的な治療介入の可能性に関する重要な洞察をもたらします。Glucose-Glo™ と Glucose Uptake-Glo™ アッセイは迅速で選択的、かつ高感度なグルコース測定の方法です。

Glucose Uptake-Glo™ Assayを使用した様々な条件下で処理された脂肪細胞におけるグルコース取り込みの測定 サイトカラシンBはグルコース輸送体阻害剤であり、グルコース取り込みを減少させます。重要なインスリンシグナル伝達酵素であるホスファチジルイノシトール3-キナーゼ(PI3K)阻害剤のLY294002は、インスリン単独に比べてグルコース取り込みを減少させます。

Glucose-Glo™ Assayを使用した糖新生の測定とインスリンによる阻害 2000個のiCell® Hepatocytes 2.0 (CDI)から形成されたマイクロ組織(InSphero)は、洗浄後、10 mM乳酸、2 μMフォルスコリン、および様々な濃度のインスリンを加え、6時間インキュベートされました。
脂質代謝の測定
肥満は、脂肪を合成・貯蔵を行う脂肪生成と、エネルギーのために貯蔵された脂質を分解する脂肪分解の間の不均衡によって特徴付けられます。これらの経路の調節不全は、過剰な脂肪蓄積と代謝機能障害につながります。脂肪生成と脂肪分解の主要なマーカーを測定することで、脂肪組織の動態に関する貴重な洞察が得られ、代謝バランスを回復するための潜在的な治療戦略を見出す手助けとなります。
弊社の脂質代謝アッセイ は、グリセロール、トリグリセリド、コレステロール、およびコレステロールエステルを検出し、脂質分解と脂質生成を測定するための高感度かつ簡便な方法です。


Glycerol-Glo™ Assayを使用したインスリン反応における脂肪分解の測定 3T3-L1 MBX脂肪細胞は洗浄後、イソプロテレノール(25 nM)およびインスリン(150 nM)の異なる組み合わせで90分間処理されました。

Triglyceride-Glo™ Assayを使用した3D肝臓マイクロ組織におけるトリグリセリドの測定 3D InSight Human Liver Microtissues(InSphero)は、生理的なグルコースおよびインスリンレベル(LG/LI)または超生理的なレベル(LG/HI)の条件下で、さらにBSAに結合した遊離脂肪酸(FFA)または低密度リポ蛋白プラズマ分画(LDL)を添加し、インキュベートされました。
Researcher Spotlight
本ブログ記事では、デューク大学のJon Campbell研究室が、当社の技術を活用してインクレチン生物学の特徴付けをどのように行っているかをご紹介します。以下の公開文献の詳細をご参照ください。これらの文献では NanoBRET™ technology を用いたリガンド誘導性Gs結合の測定、Lumit® technology を用いたインスリン及びグルカゴンの定量、さらに GloSensor™ technology を用いたcAMP量のモニタリングが実施されています。
The incretin co-agonist tirzepatide requires GIPR for hormone secretion from human islets
GLP1-mediated delivery of tesaglitazar improves glucose metabolism in mice
インクレチン関連ホルモン
GLP-1, GIPやグルカゴンといったホルモンは、代謝、食欲、エネルギーバランスの主要な調節因子であり、肥満治療薬の開発において重要なターゲットとなっています。これらのホルモンの活性を測定することは、代謝機能や治療の可能性についての貴重な洞察が得られます。
バイオアッセイを用いた受容体活性測定
弊社のバイオアッセイは、エンジニアリングされた細胞を用いてホルモン受容体の活性化を発光レポーターにリンクさせ、受容体活性の高感度かつ定量的な測定を可能にします。GLP-1、GIP、またはグルカゴンといったインクレチン関連ホルモンが各受容体に結合すると、細胞内のシグナル伝達経路がルシフェラーゼの発現を誘導し、測定可能なシグナルを生じます。このアッセイにより、研究者は受容体の機能を評価し、薬の候補分子の最適化を進め、肥満治療において重要な代謝経路を解明できるようになります。
GLP-1、GIP、グルカゴン受容体のアッセイについてはTailored R&D Solutions Team までお問い合わせください。お客様の関心に合わせたホルモン用バイオアッセイの作成もお手伝いいたします。
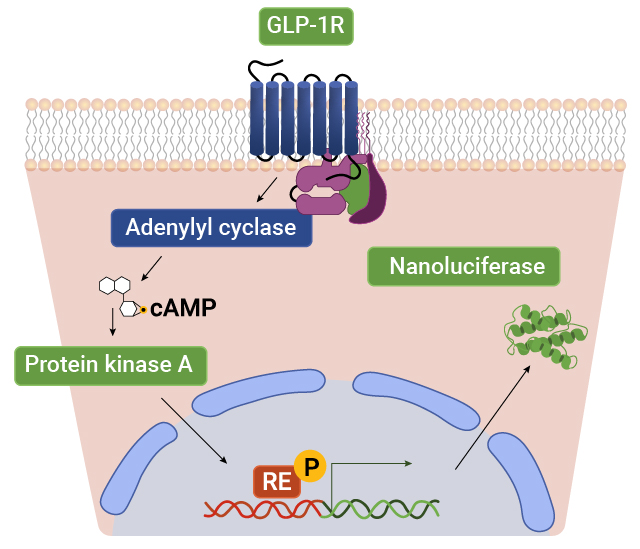
GPCRバイオアッセイの概略図 GPCRが活性化されるとアデニル酸シクラーゼがcAMPを産生し、これが引き金となりレスポンスエレメント(RE)が活性化されます。その結果、NanoLuc® ルシフェラーゼが発現し、生物発光シグナルが生じます。



各濃度のアゴニストを用いたGLP-1、GIP、Glucagonバイオアッセイ それぞれ、SemaglutideはGLP1アゴニスト、tirzepatideはGLP-1およびGIPRアゴニスト、retatrutide: GLP-1R、GIPRおよびグルカゴン受容体アゴニストです。 詳細はTailored R&D Solutionsまでお問い合わせください。
炎症
慢性炎症は肥満における代謝機能障害の主要な要因であり、脂肪組織はTNF-α、IL-6、IL-1βといったサイトカインを分泌してインスリンシグナル伝達を阻害し、病態の進行を促進します。これらのバイオマーカーを測定することは、肥満に関連する炎症を理解し、標的を絞った治療法を開発する上で非常に重要です。
主要な炎症マーカーの定量化
Lumit® Cytokine Immunoassays はシンプルかつ洗浄不要の手法でTNF-α、IL-6、IL-1βなどの主要マーカーの定量化を実現します。これらの発光アッセイを用いることで、脂肪細胞および免疫細胞におけるサイトカイン分泌を正確に測定でき、代謝機能障害における炎症の役割について貴重な洞察を得ることができます。

Lumit® Cytokine Immunoassayを用いたIL-2、IL-6、IFN-γ、TNF-αの検出 ヒトPBMCは96ウェルプレートに100µlずつ播種され、細胞刺激カクテル(CSC)、リポポリサッカライド(LPS)、またはR848で24時間処理されました。
ミオスタチン
筋肉肥大の負の調節因子であるミオスタチンは、肥満や代謝性疾患の研究において有望なターゲットとして注目されています。ミオスタチンシグナリングの阻害は、筋肉量を増加させ、エネルギー消費を高め、代謝の状態を改善する可能性があるため、肥満治療の有望なアプローチとなります。
ミオスタチン阻害の測定
弊社のミオスタチンバイオアッセイを使用すれば、ミオスタチン阻害の測定が容易に行えます。詳細はTailored R&D Solutions Team までお問い合わせください。

ミオスタチンバイオアッセイ細胞を用いたミオスタチンEC80の条件下での各濃度の抗ミオスタチン阻害抗体の阻害測定 5時間後、Bio-Glo-NL™ reagent 試薬を添加し、GloMax® Discover Microplate Readerで測定しました。
肥満研究向けのサービス
肥満研究を支援するためのカスタマイズされたツールや専門的なガイダンスが必要ですか? 弊社のTailored R&D Solutions Team がサポートいたします。弊社のサービスは以下の通りです。
カスタムアッセイ開発
- 関心のある受容体またはホルモン用のバイオアッセイの開発
- GPCR機能性アッセイ(例:リガンド結合、内在化、β-アレスチン結合)
- 肥満研究における炎症を調べるためのカスタムサイトカイン検出アッセイ
スクリーニング&プロファイリングサービス
- GPCRモジュレーター(例:アゴニスト、アンタゴニスト、バイアスリガンド)のハイスループットスクリーニング
- 代謝経路ターゲット(例:インスリンシグナル伝達、脂質代謝、エネルギーバランス)の機能性スクリーニング
- 肥満に起因する炎症の評価のためのサイトカインプロファイリング