抗体-薬物複合体 (ADC) の探索と開発
抗体-薬物複合体(ADC)研究を強化するために、あらゆる開発段階をサポートするプロメガの一連の技術をご活用ください。構想の初期段階から、詳細なin vitro有効性評価に至るまで、当社のツールは研究に不可欠な洞察を提供するよう設計されています。先進的なビーズ上での精製およびコンジュゲーションプロセスによりワークフローを効率化し、内部化効率の詳細な解析を行い、ADCの機能性と特異性を正確に評価できます。
創薬への道のりを加速するために、私たちにできることがあればぜひお知らせください。

ADCとは?
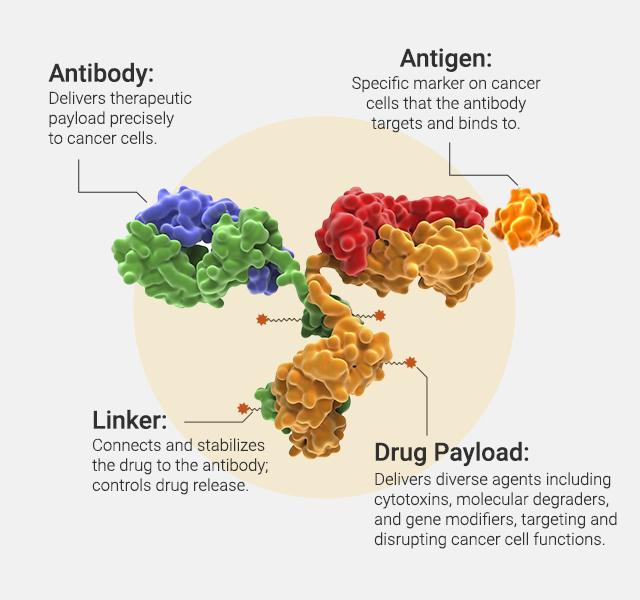
抗体薬物複合体(ADC)は、特にがん領域における標的型薬物送達技術の大きな進歩を代表しています。ADCの概念は、「抗体」「リンカー」「ペイロード」という3つの重要な要素に基づいています。抗体は、通常がん細胞の表面で過剰発現している特定の抗原を認識して結合するように設計されています。リンカーは、切断可能または切断不可能なタイプがあり、抗体に細胞毒性薬物(ペイロード)を安定に結合させます。このリンカーは血中では安定でありながら、がん細胞にADCが取り込まれた後に薬剤を放出するように設計されており、致死的な薬剤を腫瘍に直接届ける役割を果たします。ADCの探索および開発には、抗体の選定、ADCの細胞内取り込み、ペイロード機能の評価といった重要なステップが含まれます。
ADCは、モノクローナル抗体の標的指向性と、低分子薬物の強力な細胞毒性を組み合わせた治療ツールであり、腫瘍細胞を選択的に標的として殺傷し、健常組織へのダメージを最小限に抑えるよう設計されています。当社では、免疫応答を媒介するFcエフェクター機能および腫瘍細胞の直接的な殺傷に関わるペイロード機能の両方を評価する分析ツールを提供しています。これらのツールには、Fc受容体特性評価や細胞傷害性アッセイが含まれており、ADC療法の全体的な有効性と安全性の評価に役立ちます。
エンジニアリング
ビーズを利用した結合と精製
Magne® Protein G および Magne® Protein A ビーズは、抗体の効率的かつ選択的な精製のために設計されています。ADC開発においては、この技術により複雑な生体混合物から高純度の抗体を分離し、オンビーズでのコンジュゲーションが可能になります。磁性ビーズを使用することで、シンプルでスケーラブル、かつ迅速なコンジュゲーションおよび精製プロセスが実現されます。高スループット向けの Maxwell® Antibody Capture System は、KingFisher®磁性粒子プロセッサーやラボ内のリキッドハンドラーと互換性があります。あらゆるHTプラットフォームに精通した弊社フィールドサポートチームが、この化学系の成功をお手伝いします。
質量分析
質量分析 (MS) は、ADC研究において重要なツールであり、これらの複雑な治療薬の重要品質特性(CQA)を特定・定量・保証するために高い精度を発揮します。MSは以下の用途に使用されます:
- バイオ医薬品タンパク質の配列確認(ADCのコンジュゲーション部位を含む)
- 薬物対抗体比(DAR)の解析
- 生体試料中におけるADC濃度の正確な測定(前臨床および臨床)
- ADCの安定性および分解の評価
- 各ADCバッチが厳格な品質基準とロット間の一貫性を満たしていることの確認
- ホスト細胞由来タンパク質不純物のモニタリング
プロメガの 質量分析向けソリューション(プロテアーゼや標準試薬を含む)について、ぜひご覧ください。
ADC アプリケーション向けプロテアーゼ一覧
内在化
pH Reactive Dyes
pHAb Reactive Dye は、ADC研究者が抗体の細胞内取り込みを正確に追跡することを可能にします。これらの染料はエンドソームやリソソームのような酸性環境下で蛍光を発し、ADCの送達効率を定量的に評価する手段を提供します。これにより、ADCの治療効果の評価および向上に役立ちます。
本論文に掲載されたさらなるデータをご覧ください:pHセンサー蛍光染料を用いた均一プレートベースの抗体取り込みアッセイ
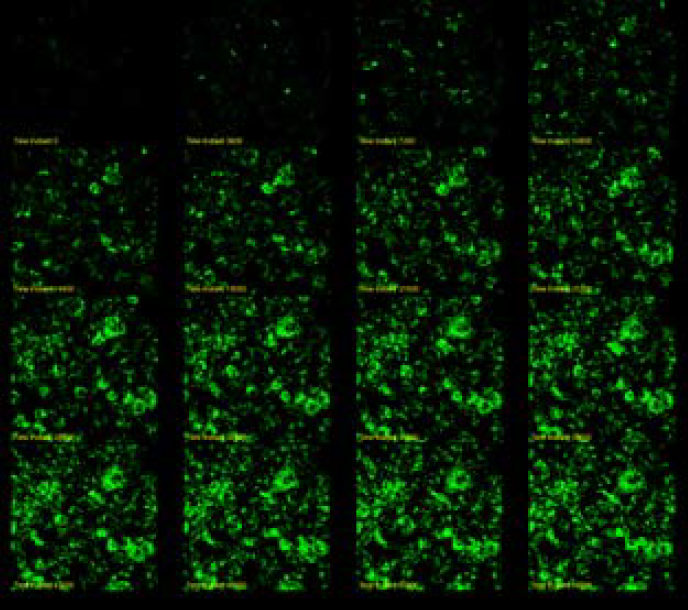
Trastuzumab (抗HER2抗体) にpHAb dyeを標識しました。SKBR3細胞に30nMのTrastuzumab-pHAb dyeを処理し、60分ごとに画像を撮影しました。
Antibody Internalization Bioassay
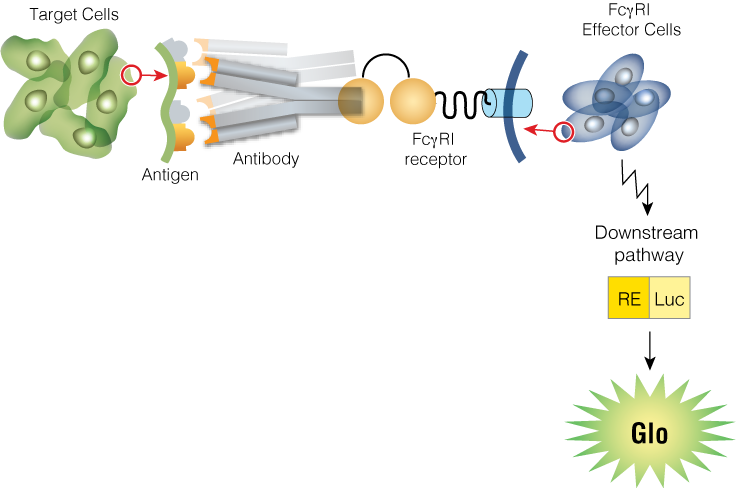
The Antibody Internalization Bioassay gives researchers an endpoint readout to monitor antibody internalization. The assay is based on an anti-Fc Fab labeled with NanoLuc® luciferase binding to a primary antibody or ADC therapeutic.
When the primary antibody binds to the target antigen, the complex is internalized, while unbound antibody is washed away. The detection reagent that includes a membrane-impermeable NanoLuc® inhibitor (Bio-Glo-NL™ Glo-Guard), a membrane-impermeable NanoLuc® inhibitor buffer (Bio-Glo-NL™ Glo-Guard Buffer, yellow shading in figure) and a membrane-permeable luciferase substrate is added to the cells. The resulting luminescent signal is primarily generated from the internalized Fab:primary antibody complex.

Accurately Compare Antibody Internalization Across Structural Variants in Adherent and Suspension Cells

The Antibody Internalization Bioassay was used to quantify the internalization of two classes of ADCs and a non-conjugated version.
Panel A. Raji target cells were plated with CD19-specific antibodies loncastuximab, a loncastuximab ADC and a control IgG.
Panel B. SKOV3 target cells were plated with HER2-specific trastuzumab, a trastuzumab ADC and a control IgG. The Antibody Internalization Bioassay is amenable to measuring internalization in both suspension (Raji) and adherent (SKOV3) cell types.
Fc受容体の特性評価
Fc受容体(FcR)との相互作用を理解することは、ADC開発において極めて重要であり、その作用機序や免疫系との関与に直接影響を与えます。この特性評価は、抗体依存性細胞傷害(ADCC)、抗体依存性貪食(ADCP)、補体依存性細胞傷害(CDC)を通じてADCの有効性を最適化し、これら先進的治療法の安全性および治療プロファイルの形成に貢献します。
ADCC and ADCP
ADCC(抗体依存性細胞傷害)は、免疫細胞が抗体でコーティングされた標的細胞を攻撃・破壊するプロセスであり、ADCP(抗体依存性貪食)は、貪食細胞が標的細胞を取り込み、消化するプロセスを指します。プロメガのFcエフェクター活性バイオアッセイは、これらのFcエフェクター機能の活性を定量的に測定するために特別に設計されており、ADC開発を導くために必要な重要なデータを研究者に提供します。
ADCCおよびADCPレポーターバイオアッセイを用いたADCのFcエフェクター活性の測定


trastuzumab(抗HER2モノクローナル抗体)、trastuzumab emtansine、またはtrastuzumab deruxtecanの連続希釈液を、ADCCバイオアッセイエフェクター細胞(左パネル)またはADCPバイオアッセイ(THP-1)エフェクター細胞(右パネル)と、SKOV3またはSKOV3/HER2ノックアウト標的細胞とともに、37℃で6時間インキュベートしました。
ADCCおよびADCPレポーターバイオアッセイを含む、プロメガのFcエフェクター活性バイオアッセイの全リストはこちら
Fc受容体の複数アイソタイプにわたる結合測定
Lumit® FcγR Binding Immunoassays は、ヒトFc受容体と抗体またはFc融合タンパク質との相互作用を測定するための、洗浄不要の新しい競合法アッセイです。
Lumit® FcRn Assay

Lumit® FcγRIIa (H131) Assay

Lumit® FcγRIIIa (V158) Assay

CDC
補体依存性細胞傷害(CDC)は、腫瘍細胞を破壊する免疫システムの能力を活用するメカニズムです。CytoTox-Glo™ Cytotoxicity Assay は、CDCを介した細胞殺傷を定量化するための強力な手法を提供し、ADCが補体系を活性化してがん細胞を標的に除去する可能性について貴重な洞察をもたらします。

ペイロードの機能



免疫原性細胞死
免疫原性細胞死(ICD)は、ADC研究において極めて重要な役割を果たします。ICDは、免疫系が腫瘍細胞を認識・攻撃する能力を高めることで、ADCの治療効果を補完します。ADCはICDを誘導し、がん抗原の放出や免疫細胞の腫瘍部位への動員を引き起こします。このプロセスは、ADCによる直接的な細胞殺傷効果を強化するだけでなく、腫瘍に対する持続的な免疫応答の促進にもつながるため、ADC療法の有効性向上における重要なメカニズムとされています。当社の専用アッセイを用いれば、ADC研究におけるICDの重要な役割を詳細に解析できます。詳細は以下の記事をご覧ください:免疫原性細胞死:損傷関連分子パターン(DAMPs)を測定する方法
Lumit® Immunoassays を使用することで、ICDに関与する重要なサイトカインを測定できます。これらのアッセイは、IL-1β、IL-6、TNF-α、IFN-γなどの主要な炎症性サイトカインを高精度かつ信頼性高く定量することが可能で、ADC療法に対する免疫応答の評価に不可欠です。Lumit® Cytokine Immunoassays の詳細はこちら

デグレーター
プロメガは、デグレーダーやPROTACsをペイロードとするADCの機能を解析するための、専用ツール群を提供しています。これらのツールにより、デグレーダーペイロードの有効性および作用機序を精密に評価することができ、タンパク質分解経路に対する包括的な理解が可能になります。詳細は、 標的タンパク質分解Webページ をご確認ください。
オリゴ
プロメガは、オリゴヌクレオチドやRNAを標的とする戦略を用いたADCペイロードの動態および治療的影響を探るためのソリューションも提供しています。これらのツールは、RNA標的型ペイロードの作用と創薬への応用に関する詳細な解析を可能にします。詳細はRNA標的化Webページをご確認ください。
特異性

関連サービス
プロメガのTailored R&D Solutionsチームとともに、ADC研究の可能性を最大限に引き出しましょう。最先端の技術を活用し、プロジェクト成功を支援する専門サービスを提供しています:
-
カスタムアッセイ開発:特定の解析ニーズに対応したオーダーメイドのアッセイ
-
スクリーニング:リード候補の特定と最適化を効率的に実施
-
作用機序解析:ADCの作用機序に関する詳細なインサイト
-
リアルタイム細胞死解析:生細胞におけるADC効果のモニタリング
-
タンパク質分解およびRNA標的解析:ペイロードの作用機構の詳細な解析
弊社のチームは、お客様固有の研究ニーズに対応し、ADC開発を前進させるためのサポート体制を整えています。




